注:この記事は、有識者個人の意見です。COVID-19有識者会議の見解ではないことに留意ください。
- 当初COVID-19は新規の重症肺炎としての報告が相次いだが、その後の科学的知見が深まるにつれ、呼吸器感染症としての側面だけでなく循環器系への影響も大きいことが判明した。臨床経過の中で動静脈血栓症、不整脈、心筋障害などの心血管系の合併症が生じることがわかっている。
- また、COVID-19発症前にも循環器系の関わりは大きく、心血管基礎疾患のある患者は同ウイルスに対して脆弱である。すなわち、感染が成立しやすい上に、重症化のリスクも高い。
- さらに、感染の急性期から回復した後も、感染者の一部で循環器系に長期にわたって感染の影響が残存していることがわかりつつある。
- COVID-19感染者の問題だけでなく、ワクチン接種の副反応として報告されている心筋炎や血栓症も問題となっている。
- 長期化するパンデミックにともなう医療全体の変化など、循環器領域で今回の感染拡大がもたらす副次的影響も無視できない。
はじめに
2019年12月に中国の武漢で最初の患者が確認されて以来、コロナウイルス2019(COVID-19)は急速に世界中に広がり、人類がスペイン風邪以来で直面した最大のパンデミックを呈している。2021年9月現在、世界中で少なくとも2億1800万人のCOVID-19感染者が確認されており[1]、これは世界人口の約2.8%に相当する。COVID-19は我々の日常生活にも影響を及ぼし、医療という枠組み内外で予期せぬ二次的影響をもたらしている。
一般に、ウイルス感染症と循環器系の密接な関係については、十分に立証されているが、重症急性呼吸器症候群コロナウイルス2型(SARS-CoV-2)感染症と効果的に戦うためには、これまでの理解では不十分であることが分かってきた。また、このパンデミックは循環器診療に二次的な影響をも及ぼしている。COVID-19が日常診療でより一般的になるにつれて、循環器診療に携わる医療従事者は、最新の知見を把握しておかなければならない。この総説では、ウイルスへの感染前、急性感染の最中、そして感染から回復後の各段階において考慮すべき心血管系の問題点を要約した。さらに、ワクチン関連事柄も含めて今回のパンデミックがもたらす副次的影響についても考察した。それぞれのテーマで、特に循環器系との関わりに焦点を当て、これまでに明らかになっていること、そして今後検討が必要な点をまとめた。
1. COVID-19の臨床経過に心血管基礎疾患が及ぼす影響
心血管系の基礎疾患は、COVID-19患者で不良な転帰のリスクである。ニューヨークの5279人の感染者を対象とした初期の前向きコホート研究によって、心血管疾患を持つ患者は、臨床経過が不良である可能性が明らかにされた。心疾患の中でも、特に心不全は重症化の最も大きなリスクの一つであった(オッズ比1.9、CI1.4~2.5)[2] 。同様に、20,133人の入院患者を対象とした英国の多施設共同研究において、慢性心疾患は併存疾患の中で最も多く、死亡率とも関連があった[3] 。同様の知見は、その他の地域からも報告されている[4-7]。さらに最近では、51の研究を含めた大規模なメタ解析により、このリスクの増加はすべての年齢層で一貫していることが示唆された[8]。
以上のように、心血管系基礎疾患を持つCOVID-19患者が重症化しやすいことが明らかになりつつあるが、心疾患にも様々な種類がある。現時点では、心疾患の中でも特に心不全が高リスクだと考えられる。米国のCOVID-19の8383人の心不全患者データベースの分析によると、実に約4人に1人が入院中に死亡している[9] 。20,954人の患者を対象とした多国籍コホート研究では、院内死亡の調整リスク比は、心不全で1.19で、重症な心不全(NYHA分類III/IV)では1.41だった[10]。心疾患の種類を区別した研究は不十分であり、今後も調査が必要である。
心血管疾患がCOVID-19の臨床経過に与える影響を踏まえると、患者の既往歴は注意深く聴取しなければならない。詳細な病歴把握が、感染の重症化リスクを適切に見積もること、そして治療を適切なタイミングで強化することを可能にする。
さらに、心疾患の既往のある患者に対してのワクチン接種も引き続き推進しなければならない。ワクチンが不足している地域では、様々な心血管疾患とその重症度に基づいて、接種対象の優先順位を決定する必要がある[11]。
2. 感染急性期における心血管系の合併症
はじめ、武漢での局地的な流行期には、SARS-CoV-2感染症は肺炎の集団発生として報告された。しかし、この感染症は他の臓器にも広く影響を及ぼすことがすぐに明らかになった。以来、免疫系と循環器系の密接な関係について改めて注目が集まっている[12]。
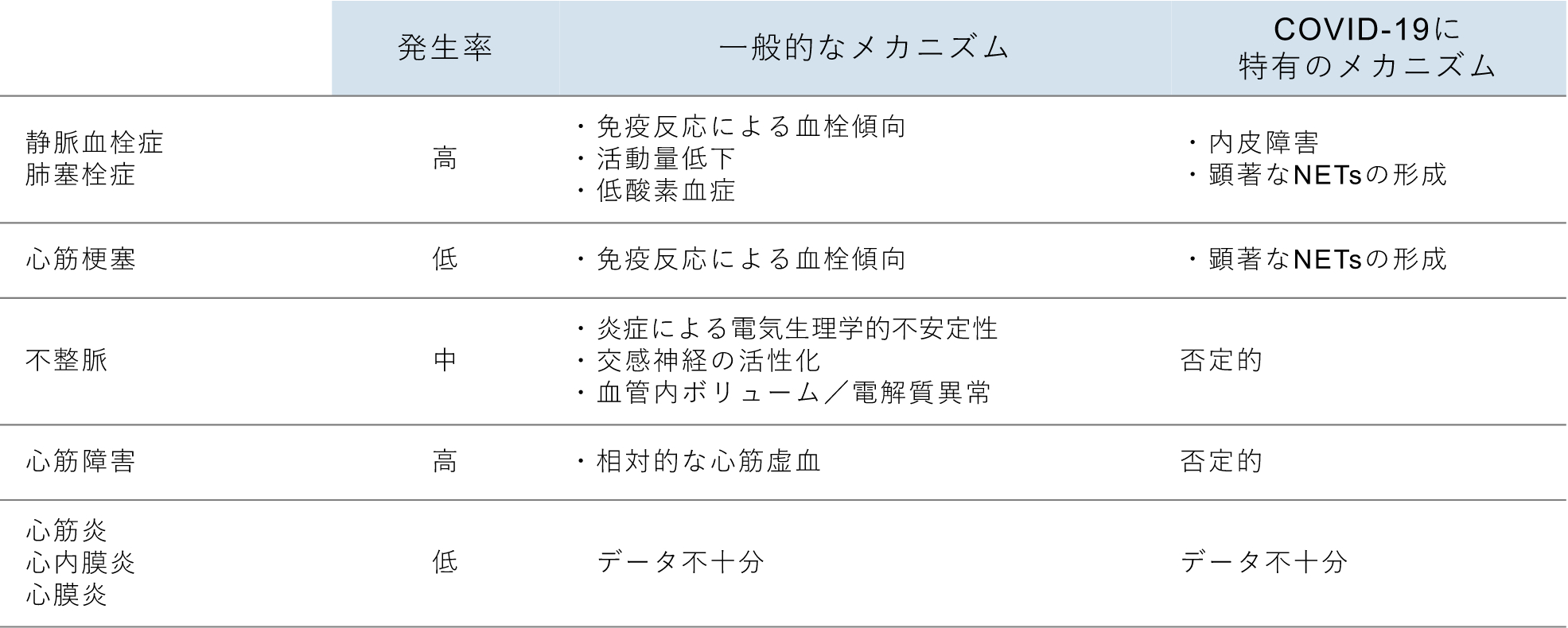
これまでの報告から、COVID-19 患者には心血管系合併症が多く発生することが分かっている。合計5815人の患者を対象とした17のコホート研究のメタ解析によると、最も一般的な心血管合併症は、心不全、心筋障害、不整脈、および急性冠症候群だった[13]。それぞれの合併症の真の発生率を推定することは困難であり、そのためCOVID-19が他の種類の感染症と比較したときどのような心血管系合併症を生じやすいのかは、現在も活発な議論が続いている。興味深いことに、最近の多国籍コホート研究では、肺塞栓症以外では、心筋炎、心筋梗塞、新規発症の心不全などの重篤な心臓合併症はまれで、入院患者のわずか2.0%にしか発生しないと指摘されている[10]【表1】。
| 表1 |
| 感染急性期における心血管系の合併症 |
 |
静脈血栓症と肺塞栓症
COVID-19患者における静脈血栓症の発症は、特に重症患者において多く報告がある[14-16]。最近の系統的レビューによると、静脈血栓塞栓症の推定発生率は7.4%であった[17] 。別の系統的レビューでは、27の研究を分析し、発生率は16.5%であると結論づけている[18] 。この大きな偏差は、研究条件のばらつきを反映したものである。研究対象者(例:疾患の重症度、患者背景)や臨床診療内容(例:抗凝固療法、造影CT検査の実施状況)の違いが要因として挙げられる。
COVID-19患者における静脈血栓症の発症には、低酸素血症や活動量低下など、他の呼吸器感染症にも共通した病因がおそらく関与している[19,20]。しかし、COVID-19では季節性インフルエンザと比較しても静脈血栓症の発生率が有意に高いことから、 COVID-19に特有のメカニズムが存在することが示唆されている[21]。ここでは、アンジオテンシン変換酵素2(ACE2)受容体が独特な役割を担っている。SARS-CoV-2ウイルスはACE2受容体を介して血管内皮に侵入し、血小板の接着と凝集に関与するvon Willebrand因子(vWF)を露出させて血栓症を引き起こす[22-25]。また、好中球もACE2受容体を発現しており、ウイルスによる活性化で好中球細胞外トラップ(NETs)を放出する[12]。NETsもまた、凝固カスケードを誘発する、免疫血栓症の重要なメディエーターである[26]。実際に、COVID-19患者の血中好中球と肺検体に関する研究では、顕著なNET形成がCOVID-19の特徴であることが示唆されている[27,28]。
このような血栓性合併症を予防するためにどのような抗凝固療法を行うべきか、未だに結論は出ていない。パンデミックの初期から、COVID-19患者に対する予防的抗凝固療法が実施されており、中国の重症COVID-19患者449人の後ろ向き研究で、低分子量ヘパリン(LMWH)による抗凝固療法が予後改善と関連していることが示された[29]。これを受けて、いくつかの学術学会は、禁忌のないすべてのCOVID-19入院患者でLMWHによる予防的抗凝固療法を推奨した[30,31]。その後の米国の大規模コホート研究によってもこの戦略が正当化された[32]。この研究により、早期のヘパリン予防投与は、重篤な出血のリスクを増加させることなく、生存可能性を34%増加させることが明らかになったのだ。しかし、予防的抗凝固療法にも関わらず依然として静脈血栓症の発生率は高く[33]、より高用量の抗凝固療法の是非が、疑問として残っていた。
最新の無作為化臨床試験(RCT)の結果を鑑みると、(予防用量以上の)治療用量でのルーチンの抗凝固療法に対しては慎重にならざるを得ない。INSPIRATION RCTは、集中治療室(ICU)で治療を受けたCOVID-19患者562人を対象に、中用量と、標準予防用量の抗凝固療法の効果を比較した臨床試験だ[34]。この試験で、中用量抗凝固療法は、血栓症、体外式膜酸素化(ECMO)治療、死亡率などの複合的な転帰に改善をもたらさないことが明らかにされた。それどころか、出血合併症がより多く生じた。ACTION RCTという、D-ダイマー高値のCOVID-19患者を治療用量または予防用量の抗凝固療法に無作為に割り付けた臨床試験でも同様の結果が得られた[35]。この試験でも、治療的用量の抗凝固療法によって臨床転帰は改善せず、予防的用量と比較して出血を有意に増加させた。この2つのRCTとは対照的に、REMAP-CAP、ACTIV-4a、ATTACCのマルチプラットフォームRCTでは、治療量による抗凝固療法が疾患の重症度によっては有用である可能性が示唆されている[36,37]。この研究では、治療用量の抗凝固療法は、非重症患者の生存率を改善する一方、重症患者の生存率は改善しなかった。また、非重症患者において、生存率の改善効果はD-ダイマー値が高い患者においてより顕著であった。以上の3つのRCTから、疾患の重症度、D-ダイマー値、出血リスクに基づいた、患者ごとの個別調整が重要であることが再確認された。
さらに、COVID-19患者で肺塞栓症(PE)をどのように診断するべきかについても結論は出ていない。特に、造影CT検査を行う患者を選別するためのD-ダイマーの閾値については、まだ議論が分かれるところである。造影CTは、PEの標準的な診断ツールとなっている一方で、その過剰使用による放射線被曝や造影剤腎症が問題視されている[38]。また、COVID-19感染者の場合は、医療従事者がウイルスに暴露するリスクもある。従来から使われているカットオフ値(500または100ng/mL)は低すぎると主張する研究者もいれば、カットオフ値を高く設定することで検査感度が低下すると主張する研究者もいる[18,39,40]。さらに、COVID-19患者でのWells基準のような検査前予測スコアの有効性を疑問視する声もある[41,42]。COVID-19患者でのPEの発症率が高いことを考えると、信頼できるエビデンスが蓄積するまでは、造影CT検査を実施する閾値は低く設定しておくことが妥当かもしれない。
心筋梗塞
パンデミックの初期段階から、複数のコホート研究によって、COVID-19が急性心筋梗塞(AMI)を誘発することが示されている[15,43]。5119人のCOVID-19患者を対象としたデンマークの研究では、COVID-19診断後の14日間にAMIの発生率が5倍高くなると推定した[44]。また、86742人の患者記録を分析したスウェーデンの全国調査でも、COVID-19発症後の最初の1週間のAMIの発生率は、対照区間と比較して2.9倍であり、COVID-19患者は、発症後2週間の心筋梗塞の発症オッズ比がコントロールと比較して3.4であった [45]。これらの研究により、COVID-19患者は、特に感染から2週間以内にAMI発症のリスクが高いことが確認された。
COVID-19におけるAMI発症の詳細なメカニズムは明らかではないが、一般的に感染は動脈硬化性プラークへの炎症性細胞浸潤、血小板活性化、冠血管収縮、内皮機能障害など複数の機序によって冠動脈血栓症を誘発する可能性がある[46] 。実際、呼吸器感染症が急性冠症候群のリスクを高めることは、過去の文献で検証されている[47-49]。16の症例対照研究のメタ解析によると、インフルエンザを含む呼吸器感染症は、AMIの発症と有意に関連していた[50] 。また、COVID-19患者では、先述のNET形成も特異的な役割を演じている可能性がある。COVID-19感染後のAMI患者5人とCOVID-19非感染の対照AMI患者50人での吸引された冠動脈血栓を比較した症例集積研究では、COVID-19患者全員からNETが検出されたのに対し、対照群では68%のみ陽性であった[51]。また、NET密度の中央値もCOVID-19患者で有意に高かった(61% vs. 19%)。
COVID-19患者のAMIの治療方針は、非COVID-19患者のものと基本的に同じであるが、患者との接触制限には留意しなければならない[52]。COVID-19陰性が証明されていない限り、緊急の冠動脈造影(CAG)は適切な個人用保護具を装着したうえで、最小限のスタッフで実施する必要がある。
COVID-19感染に誘発されたAMIは、今後冠動脈リスクの高い人々の間で問題になるかもしれない。先述のメタ解析の著者らは、AMI予防におけるインフルエンザワクチンの効果を分析した結果、その効果は数値として29%で、スタチン(36%)や降圧薬(15~18%)などの他の予防策に匹敵すると推定している[50]。このように、ワクチン接種のメリットは、ウイルス感染自体の予防だけでなく、心血管系の合併症を防ぐことにもある。
不整脈
COVID-19の急性期には、様々な不整脈が起こり得る。ある世界的調査によると、COVID-19に合併する最も一般的な不整脈は心房細動で、回答者683人中142人(21%)から報告された[53]。その一方で、致死的な不整脈はほとんど報告されておらず、例えば、悪性の心室頻拍と心室細動の報告は、回答者のわずか4.8%に留まった。4526人のCOVID-19患者の症例集積研究では、18%が入院中に不整脈を発症していた [54] 。不整脈を発症した患者のうち、心房性頻拍の発生率は 81.8%、心室性頻拍の発生率は 20.7%であった。なお、不整脈に関する初期の報告は、その合併頻度(特に心室頻拍)を過大評価した可能性がある。というのも、かつてはヒドロキシクロロキンやアジスロマイシンの使用によって薬物性のQT延長とTorsade de Pointesが多く生じていたのだ [55] 。現在、これらの薬剤の有効性は否定され、もはや使用されることはなくなっている。
不整脈発症の病態生理はまだ不明であるが、全身性の免疫炎症反応によって促進されるものと思われる。炎症性サイトカインは心筋の活動電位期間(APD)を延長させるため、心電図上QT間隔が長くなる。これが交感神経活性化と相まって、心室性不整脈を誘発する可能性がある。また、サイトカインは、遅延性脱分極(DAD)を誘発し、異所性活動の頻度を増加させ、心房性不整脈の原因にもなる[56-58]。他の要因として、電解質異常や重症COVID-19患者における血管内ボリュームの不均衡も考えられる。
このような仮定に基づけば、不整脈の頻度は感染の重症度と関連していることが想定され、実際、前述の症例集積研究では、不整脈を発症した患者の43%が機械的人工呼吸を受けていた[54] 。さらに、700人のCOVID-19患者の分析では、ICUで治療を受けている患者は、一般病棟の患者に比べて不整脈の発症が10倍多いことが示された[59]。集中治療を受けている患者の悪性不整脈は、予後不良の指標である心筋傷害とも関連していた[60]。
その他の合併症
COVID-19におけるその他の心血管系合併症として、心内膜炎、心膜炎および心筋炎が報告されている。心内膜炎と心膜炎の報告は、症例報告に限られている[61,62]。心筋炎を疑う手がかりの一つである心筋傷害はCOVID-19患者でよく見られるが、心電図や心エコーでの異常所見など、その他の臨床的特徴を伴っていることは少ない[17,63]。
心筋障害と心血管バイオマーカー
心筋障害とは、通常(病態に関係なく)心筋トロポニン上昇を指す。これまでの研究で、この所見はCOVID-19患者では頻度が高いことが分かっている。トロポニン上昇の発生率は、4.8~54%と報告によって大きく異なっている[17]。
トロポニン値は、COVID-19の重症度と死亡率に密接に関係している。中国からの初期の報告では、心筋傷害はICU患者でより多く見られた(22.2%対2.0%)[64]。さらに、トロポニン上昇は、死亡率だけでなく、敗血症、急性腎不全、大出血などの合併症の発生とも関連していた[65]。別の多施設共同研究では、大多数の患者でトロポニンIは軽度(例えば0.03~0.09ng/ml未満)の上昇だが、わずかな上昇であっても死亡率と有意に関連することが報告された[66]。意外なことに、もともとの心血管疾患の既往がなく心筋損傷を示すCOVID-19患者は、心血管疾患の既往があるが心筋損傷を示さない患者と比較して、予後が悪かった[60]。
心筋傷害と重症化との関連は、COVID-19に限ったことではなく、市中肺炎や季節性インフルエンザなど他の感染症でも以前に示されている[67,68]。H7N9 インフルエンザの入院患者の研究では、45.8%がトロポニンの上昇を示し、心筋障害は院内死亡率と関連していた[68]。さらに、トロポニンは、早期敗血症の重症患者[69]や他の急性呼吸器疾患[70]の予後指標として提案されている。
COVID-19における心筋傷害は、通常、免疫反応が惹起した全身性炎症による、心筋への酸素の需要供給不均衡の結果と考えられる。そのような全身性の病態以外に、ウイルスの心筋への直接侵入を示唆する研究も散見されるが、現時点では根拠が不足している。例えば、いくつかの in vitro 研究で、ヒト iPS 由来の心筋細胞は SARS-CoV-2 に直接感染しやすいことが示唆されている [71,72]。しかし、COVID-19 患者の心筋組織では、高ウイルス量のSARS-CoV-2 が41%で確認されたが、それは心筋細胞ではなく間質で検出されたものだった[73]。また、これはウイルスを検出しただけで、炎症細胞浸潤の併発は認めなかった。
日常的に循環器診療で使用されている他のパラメータも、COVID-19の予後予測に有効である可能性がある。そのようなバイオマーカーの一つがD-ダイマーである。COVID-19患者191人を対象とした初期の研究では、D-ダイマーが1μg/mLを超えると、院内死亡率が上昇した[74]。N末端プロ脳性ナトリウム利尿ペプチド(NT-proBNP)は、現在研究されているもう一つのバイオマーカーである。スペインの患者3080人を対象とした大規模コホート研究において、NT-proBNPは、関連する交絡因子を調整しても死亡率と独立に関連していた[75]。ただし、予後マーカーとしてこれらのバイオマーカーをルーチンとして測定することは、過剰検査にもつながるため一概には推奨されない。心筋トロポニンの場合、重度の炎症反応による相対的心筋虚血以外にも、急性冠症候群、心疾患既往、腎障害、種々の心筋症などの他の機序が関与している場合がある。このように、バイオマーカー検査結果の解釈は容易ではなく、検査結果自体に惑わされないためにも、身体診察や他の診断ツールを用いて総合的に検討する必要がある。
3. 心血管系への長期的影響
COVID-19からの回復に成功した患者でも、感染後に症状が持続することがある。COVID-19の慢性期における合併症は「long COVID」と呼ばれ、研究の対象になっている。COVID-19 回復者179 名を対象としたアンケートでは、87.4%の回答者が少なくとも 1 つの症状の持続を報告している[76]。最も頻度の高い症状は、疲労(53%)、呼吸困難(43%)、関節痛(27%)、および胸痛(21%)であった。
循環器関連では、心筋炎症の持続が問題として提起されている。COVID-19感染歴のある若いアスリート1597人を対象とした大規模コホート研究によると、2.3%の回復者が心血管磁気共鳴(CMR)画像で心筋炎を疑う所見を認めた[77]。ただし、実際に臨床的な心筋炎を呈していたのは0.31%に過ぎなかった。他の研究でも、急性感染から数ヵ月後にも心筋の炎症が進行している可能性が示唆されている。あるコホート研究では、約2〜3ヶ月後のCMR画像で回復者の実に78%がT1またはT2の異常所見を示していた[78]。また、入院中にトロポニン陽性を示した感染者148人の研究では、26%がCMR画像で心筋炎様のパターンを呈していた[79]。これら2つの研究では、左室収縮率はおおよそ維持されていたが、別の研究では、潜在的な心機能不全を検知するのにより感度の高いマーカーである、左室長軸方向グローバルストレイン(LVGLS)が、軽症患者であっても低下している可能性が示唆されている[80]。
感染症による後遺症はCOVID-19に限った話ではない。例えば、市中肺炎の患者では、症状の消失まで1ヶ月以上を要する[81]。症状はさておき、合併症の発生という側面についても、感染症罹患後10年経った時点でも心血管リスクは高くなっているという報告も存在する[82]。今後も出てくるであろう、COVID-19回復者の長期追跡調査によって、感染後の診療継続の必要性の有無が明らかになると期待される。
4. 循環器診療への副次的影響
循環器疾患の疫学への影響
今回のパンデミックは、多くの疾患の疫学やその発症様式にまで影響を及ぼしている[83,84]。循環器診療に話を絞ると、厳しい感染対策措置がとられたパンデミックの第一波の最中に、急性発症の心血管疾患の疫学が大きな影響を受けた。オーストリアの全国的な後ろ向き研究では、2020年3月初旬の流行後、急性冠症候群の入院が39.4%減少した[85]。同様の傾向は、英国、イタリア、米国でも確認されている[86-88]。しかし、入院患者数が減少した一方、全体的な心血管死亡は増加したことが明らかになっている。ニューヨークでは、2020年1~6月までの虚血性心疾患による死亡は、2019年の同時期の2.39倍であった[89]。英国の大規模な研究によると、パンデミックは2085(+8%)の過剰な急性心血管死を引き起こし、そのほとんどが自宅で発生していた[90]。英国での別の研究では、血栓塞栓症による死亡が病院内ではなく院外で増加したことが確認された[91]。これらの病院外での急性心血管イベントによる死亡率の増加は、通院によるウイルス暴露を患者側が恐れたことや、パンデミックの初期段階に医療体制がひっ迫していたことが原因かもしれない。
座って過ごしがちな在宅生活への移行もまた、心血管疾患の疫学変化をもたらしているかもしれない。身体活動の重要性は、あらゆる種類の心血管疾患において十分に立証されている[92] 。パンデミックの中、急性静脈血栓塞栓症(VTE、すなわち肺塞栓症と深部静脈血栓症)が特に懸念されている。中国の多施設共同研究では、3358人のVTE患者を対象に、パンデミック前とパンデミック中の患者でVTEの危険因子の変化を評価した。対照期間と比較して、外傷や手術によるVTEの割合はパンデミック期間中に低く、一方で、運動不足によるVTEの割合はパンデミック期間中に有意に高かった(30.7%対22.6%)[93]。COVID-19への対抗策が異なる他の地域でも、同様の観察結果が得られている[91,94,95]。
外出禁止令などの厳格なソーシャルディスタンスの取り決めは、感染が拡大している地域では必要な措置である。しかし、運動不足は心血管疾患の発症と進行につながるだけでなく、ウイルスに暴露した際の感染リスクまで高める[96,97]。行動制限を要求するような政策を実施する場合は、身体活動量の低い生活のリスクを強調し、定期的に運動するよう促すことが重要である。
循環器外来診療への影響
患者の行動変化による長期的な影響についても、懸念が高まっている[98]。まず一つに、慢性心疾患を持つ患者は、医療機関への受診を避けるようになっている[99]。定期的な外来診療は的確な処方調整を可能にし、心血管疾患の予後の改善とも関連している[100,101]。さらに、パンデミックの影響で健康診断や検査も少なくなり、診断や治療介入に遅れが生じている[84]。一般市民に対して、適切な医療受診の重要性を強調する必要がある。
臨床医の中には、このパンデミックを医療分野におけるデジタル変革の機会として捉える人もいる。たとえば、患者と医師の接触を避けるため、循環器外来診療では情報通信技術(ICT)が推進されている[102]。しかし、新しい技術の活用にはアクセシビリティの問題がついてまわる。ある研究では、パンデミック中に遠隔診療を受ける予定だった2940人の心血管疾患患者の特徴を分析した[103]。ビデオ遠隔診療を実際に完了できた人々は、これを活用しなかった人々に比べて、男性の割合が有意に多く、所得が高かった。ICTを利用したヘルスケアへの流れは今後も続くだろうが、デジタルデバイドの問題がその律速段階となるかもしれない。
ワクチンによる副反応
COVID-19ワクチンはパンデミックにいち早く対処するために急速に開発された。デルタ株のような感染性の高い新型株の流行が生じているにも関わらず、ワクチンは重症化を予防できている[104]。これらのワクチンは、迅速な開発と大量生産を達成するために、比較的新しい技術を採用した[105]。抗原そのものではなく、抗原の遺伝情報(mRNAまたはDNA) を免疫系に導入するものである。発生率は極めて低いと思われるが、心筋炎および血栓症の副作用が懸念されている【図1】。
| 図1 |
| ワクチンによる副反応(心筋炎および血栓症) |
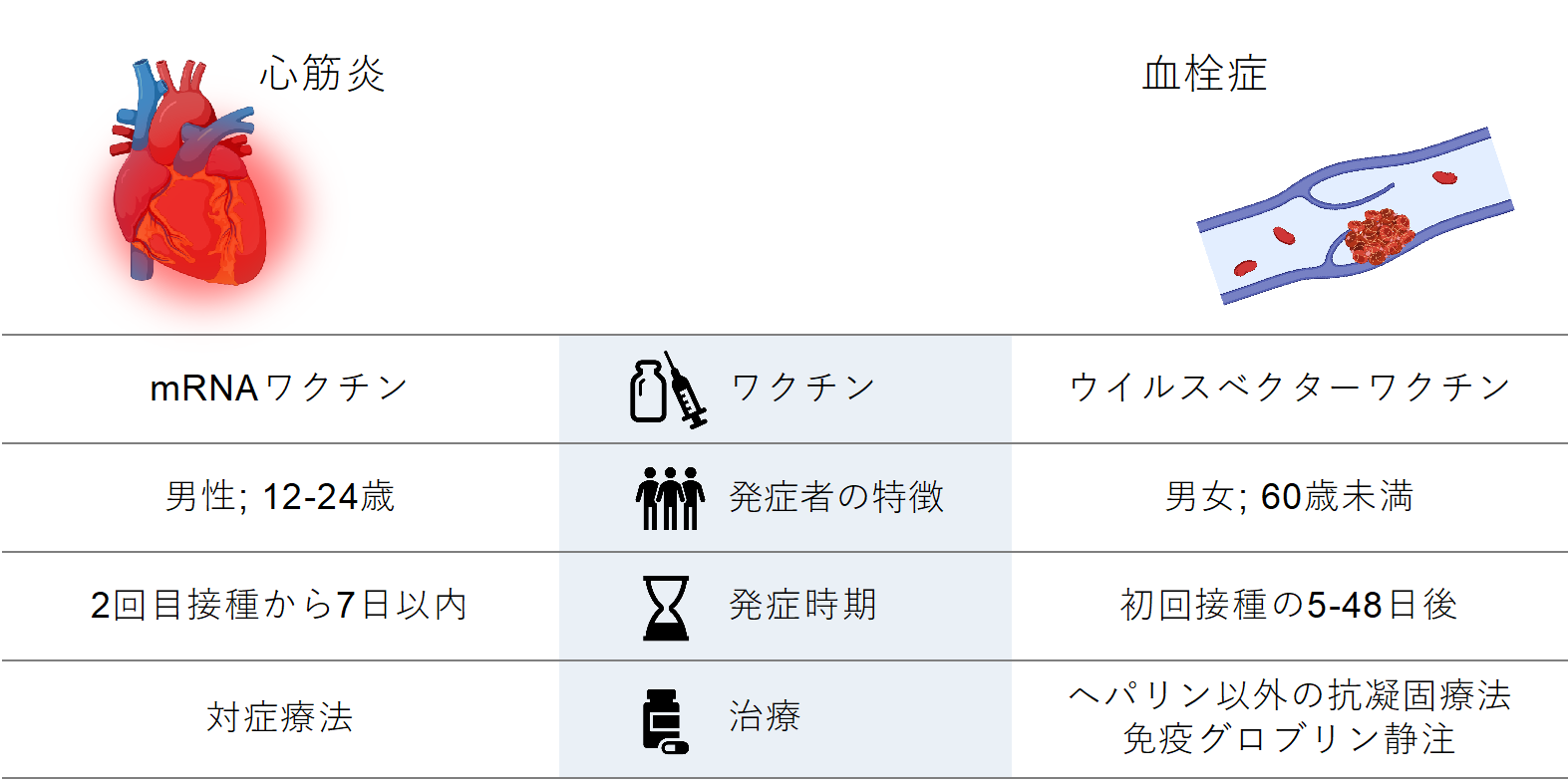 |
急性心筋炎は、ファイザーとモデルナのmRNAワクチンを接種された人で報告されている。アメリカ疾病予防管理センター(CDC)のワクチン安全性監視システムに基づく解析によると、2021年6月現在、ワクチン接種後の心筋炎の報告は1226件ある[106]。これらは、若い男性(12~24 歳で最も多い)で、2 回目の接種後に多く発生した。92%が1週間以内の発症で、発症までの期間の中央値は2日であった。通常、急性の胸痛とトロポニン値の大幅な上昇を認める[107,108]。また、臨床経過は大半が軽度であり、少なくとも短期的な予後は非常に良好であることが判明している[109]。この有害事象の発生率はまだ調査中であるが、ワクチンの有益性はその危険性を明らかに上回っている。CDCの予防接種の実施に関する諮問委員会は、若年者に限っても、100万回の接種あたりで、560件のCOVID-19入院と138件のICU入室が避けられるのに対し、心筋炎の発症は40件にすぎないと推定している[106]。
血小板減少症を伴う血栓症は、ウイルスベクターワクチンの初回接種後に発生している。このタイプに分類されるワクチンは、アストラゼネカ製のワクチンとジョンソン&ジョンソン製のワクチンである。この症候群は、ワクチン誘発性免疫性血小板減少症および血栓症(VITT)と呼ばれるようになっている[110]。報告された症状は、多くの点でヘパリン起因性血小板減少症(HIT)に類似している。この副作用の発症者は、ヘパリンに暴露されていないにもかかわらず、HITで検出される抗体抗血小板因子4(PF4)抗体が陽性であった。294名のVITT症例を対象とした最近のコホート研究によると、患者は比較的若く(85%は60歳未満)、初回ワクチン接種後5〜48日で発症した[111]。死亡率は22%で、脳静脈洞血栓症や重度の凝固異常を有する患者で死亡率が高かった。HIT治療からの推測に基づき、免疫グロブリン静注や非ヘパリン系抗凝固薬の投与が治療法として推奨される[112,113]。初期治療への反応が悪い場合には、血漿交換も考慮される[114]。mRNAワクチンの場合と同様、世界保健機関(WHO)は、ワクチン接種の利点が潜在的リスクよりも明らかに大きいと結論づけている[113]。
この前例のない規模のワクチン接種キャンペーンにおいて、安全性モニタリングが重要であることは間違いない。しかし、これまでの報告によると、ワクチンから得られる利益は、そのリスクよりはるかに大きい。実際、最新の研究では、心血管イベント(心筋炎と血栓症)の発症リスクは、ワクチン接種後よりもSARS-CoV-2感染後の方が高いことが示されている[115,116]。ワクチン接種に関する合理的な意思決定を可能にするためには、一般の報道機関ではなく、CDCやWHOなどの信頼できる情報源からの最新の安全性ガイダンスを常に把握しておくことが重要である。
結論
COVID-19と循環器系の密接な関係に関して、注目すべき複数のトピックを解説した。COVID-19は、その感染のすべての段階において、循環器系疾患と関連していることがわかった。さらに、このパンデミックは循環器診療に重大な二次的影響を及ぼしていることも明らかにした。この分野は急速に変化しているため、この総説で述べた内容は短期間のうちに改訂される可能性があり、最新の知見には目を光らせ続けなければならない。新しい知識と経験を積み重ねていくことで、我々はこのパンデミックからより強く立ち上がることができるだろう。
[引用文献]
- WHO COVID-19 Dashboard. Available from: https://covid19.who. int/[Accessed: 1st September 2021]
- Petrilli CM, Jones SA, Yang J, Rajagopalan H, O’Donnell L, Chernyak Y, et al. Factors associated with hospital admission and critical illness among 5279 people with coronavirus disease 2019 in New York City: Prospective co- hort study. BMJ 2020;369:m1966.
- Docherty AB, Harrison EM, Green CA, Hardwick HE, Pius R, Norman L, et al. Features of 20 133 UK patients in hospital with covid-19 using the ISARIC WHO Clinical Characterisation Protocol: prospective observational co- hort study. BMJ 2020;369:m1985.
- Matsunaga N, Hayakawa K, Terada M, Ohtsu H, Asai Y, Tsuzuki S, et al. Clin- ical epidemiology of hospitalized patients with coronavirus disease 2019 (COVID-19) in Japan: Report of the COVID-19 Registry Japan. Clin Infect Dis 2020:ciaa1470.
- Chen J, Qi T, Liu L, Ling Y, Qian Z, Li T, et al. Clinical progression of patients with COVID-19 in Shanghai, China. J Infect 2020;80:e1–6.
- de Souza WM, Buss LF, Candido D da S, Carrera J-P, Li S, Zarebski AE, et al. Epidemiological and clinical characteristics of the COVID-19 epidemic in Brazil. Nature Hum Behav 2020;4:856–65.
- Grasselli G, Zangrillo A, Zanella A, Antonelli M, Cabrini L, Castelli A, et al. Baseline characteristics and outcomes of 1591 patients infected with SARS-CoV-2 admitted to ICUs of the Lombardy region, Italy. JAMA 2020;323:1574.
- Bae S, Kim SR, Kim M-N, Shim WJ, Park S-M. Impact of cardiovascular disease and risk factors on fatal outcomes in patients with COVID-19 according to age: a systematic review and meta-analysis. Heart 2021;107:373–80.
- Bhatt AS, Jering KS, Vaduganathan M, Claggett BL, Cunningham JW, Rosen- thal N, et al. Clinical outcomes in patients with heart failure hospitalized with COVID-19. JACC Heart Fail 2021;9:65–73.
- Linschoten M, Uijl A, Schut A, Jakob CEM, Romão LR, et al., CAPACITY-COVID collaborative consortium and LEOSS Study Group Clinical presentation, dis- ease course and outcome of COVID-19 in hospitalized patients with and with- out pre-existing cardiac disease – a cohort study across sixteen countries. medRxiv 2021 2021.03.11.21253106.
- Driggin E, Maddox TM, Ferdinand KC, Kirkpatrick JN, Ky B, Morris AA, et al. ACC health policy statement on cardiovascular disease considerations for COVID-19 vaccine prioritization. J Am Coll Cardiol 2021;77:1938–48.
- Stark K, Massberg S. Interplay between inflammation and thrombosis in car- diovascular pathology. Nat Rev Cardiol 2021;18:666–82.
- Kunutsor SK, Laukkanen JA. Cardiovascular complications in COVID-19: a sys- tematic review and meta-analysis. J Infect 2020;81:e139–41.
- Lodigiani C, Iapichino G, Carenzo L, Cecconi M, Ferrazzi P, Sebastian T, et al. Venous and arterial thromboembolic complications in COVID-19 patients admitted to an academic hospital in Milan, Italy. Thromb Res 2020;191:9–14.
- Bilaloglu S, Aphinyanaphongs Y, Jones S, Iturrate E, Hochman J, Berger JS. Thrombosis in hospitalized patients with COVID-19 in a New York City health system. JAMA 2020;324:799.
- Poissy J, Goutay J, Caplan M, Parmentier E, Duburcq T, Lassalle F, et al. Pul- monary embolism in patients with COVID-19. Circulation 2020;142:184–6.
- Pellicori P, Doolub G, Wong CM, Lee KS, Mangion K, Ahmad M, et al. COVID-19 and its cardiovascular effects: a systematic review of preva- lence studies. Cochrane Database Syst Rev 2021;3:CD013879.
- [Suh YJ, Hong H, Ohana M, Bompard F, Revel M-P, Valle C, et al. Pulmonary embolism and deep vein thrombosis in COVID-19: a systematic review and meta-analysis. Radiology 2021;298:E70–80.
- Gupta N, Zhao Y-Y, Evans CE. The stimulation of thrombosis by hypoxia. Thromb Res 2019;181:77–83.
- Pottier P, Hardouin JB, Lejeune S, Jolliet P, Gillet B, Planchon B. Immobiliza- tion and the risk of venous thromboembolism. A meta-analysis on epidemio- logical studies. Thromb Res 2009;124:468–76.
- Piroth L, Cottenet J, Mariet A-S, Bonniaud P, Blot M, Tubert-Bitter P, et al. Comparison of the characteristics, morbidity, and mortality of COVID-19 and seasonal influenza: a nationwide, population-based retrospective cohort study. Lancet Resp Med 2021;9:251–9.
- Varga Z, Flammer AJ, Steiger P, Haberecker M, Andermatt R, Zinker- nagel AS, et al. Endothelial cell infection and endotheliitis in COVID-19. Lancet 2020;395:1417–18.
- Hoffmann M, Kleine-Weber H, Schroeder S, Krüger N, Herrler T, Erichsen S, et al. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell 2020;181:271–280.e8.
- Ackermann M, Verleden SE, Kuehnel M, Haverich A, Welte T, Laenger F, et al. Pulmonary vascular endothelialitis, thrombosis, and angiogenesis in Covid-19. N Engl J Med 2020;383:120–8.
- Ruggeri ZM. The role of von Willebrand factor in thrombus formation. Thromb Res 2007;120(Suppl. 1):S5–9.
- von Brühl M-L, Stark K, Steinhart A, Chandraratne S, Konrad I, Lorenz M, et al. Monocytes, neutrophils, and platelets cooperate to initiate and prop- agate venous thrombosis in mice in vivo. J Exp Med 2012;209:819–35.
- Veras FP, Pontelli MC, Silva CM, Toller-Kawahisa JE, de Lima M, Nasci- mento DC, et al. SARS-CoV-2–triggered neutrophil extracellular traps mediate COVID-19 pathology. J Exp Med 2020;217:e20201129.
- Nicolai L, Leunig A, Brambs S, Kaiser R, Joppich M, Hoffknecht M, et al. Vas- cular neutrophilic inflammation and immunothrombosis distinguish severe COVID-19 from influenza pneumonia. J Thromb Haemost 2021;19:574–81.
- [Tang N, Bai H, Chen X, Gong J, Li D, Sun Z. Anticoagulant treatment is asso- ciated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. J Thromb Haemost 2020;18:1094–9.
- [Moores LK, Tritschler T, Brosnahan S, Carrier M, Collen JF, Doerschug K, et al. Prevention, diagnosis, and treatment of VTE in patients with coronavirus disease 2019. Chest 2020;158:1143–63.
- [Thachil J, Tang N, Gando S, Falanga A, Cattaneo M, Levi M, et al. ISTH interim guidance on recognition and management of coagulopathy in COVID-19. J Thromb Haemost 2020;18:1023–6.
- Rentsch CT, Beckman JA, Tomlinson L, Gellad WF, Alcorn C, Kidwai-Khan F, et al. Early initiation of prophylactic anticoagulation for prevention of coron- avirus disease 2019 mortality in patients admitted to hospital in the United States: cohort study. BMJ 2021;372:n311.
- Llitjos J, Leclerc M, Chochois C, Monsallier J, Ramakers M, Auvray M, et al. High incidence of venous thromboembolic events in anticoagulated se- vere COVID-19 patients. J Thromb Haemost 2020;18:1743–6.
- Mazloomzadeh S, Khaleghparast S, Ghadrdoost B, Mousavizadeh M, Baay MR, Noohi F, et al. Effect of intermediate-dose vs standard-dose prophylactic an- ticoagulation on thrombotic events, extracorporeal membrane oxygenation treatment, or mortality among patients with COVID-19 admitted to the in- tensive care unit. JAMA 2021;325:1620.
- Lopes RD, de Barros E, Silva PGM, Furtado RHM, Macedo AVS, Bronhara B, Damiani LP, et al. Therapeutic versus prophylactic anticoagulation for pa- tients admitted to hospital with COVID-19 and elevated D-dimer concen- tration (ACTION): an open-label, multicentre, randomised, controlled trial. Lancet 2021;397:2253–63.
- Goligher EC, Bradbury CA, McVerry BJ, et al., REMAP-CAP Investiga- tors; ACTIV-4a Investigators; ATTACC Investigators Therapeutic anticoagula- tion with heparin in critically ill patients with Covid-19. N Engl J Med 2021;385:777–89.
- Lawler PR, Goligher EC, Berger JS, et al., ATTACC Investigators; AC- TIV-4a Investigators; REMAP-CAP Investigators Therapeutic anticoagulation with heparin in noncritically ill patients with Covid-19. N Engl J Med 2021;385:790–802.
- Kline JA, Garrett JS, Sarmiento EJ, Strachan CC, Courtney DM. Over-testing for suspected pulmonary embolism in American emergency departments. Circ Cardiovasc Qual Outcomes 2020;13:1–10.
- Korevaar DA, Aydemir I, Minnema MW, Azijli K, Beenen LF, Heijmans J, et al. Routine screening for pulmonary embolism in COVID-19 patients at the emer- gency department: impact of D-dimer testing followed by CTPA. J Thromb Thrombolysis 2021. doi:10.1007/s11239-021-02508-1.
- Kwee RM, Adams HJA, Kwee TC. Pulmonary embolism in patients with COVID-19 and value of D-dimer assessment: a meta-analysis. Eur Radiol 2021;9:1–19.
- Kirsch B, Aziz M, Kumar S, Burke M, Webster T, Immadi A, et al. Wells score to predict pulmonary embolism in patients with coronavirus disease 2019. Am J Med 2021;134:688–90.
- Silva B, Jorge C, Rigueira J, Rodrigues T, Silverio Antonio P, Morais P, et al. Wells and Geneva decision rules to predict pulmonary embolism: can we use them in Covid-19 patients? EHJ Cardiovasc Imaging 2021;22 jeab111.009.
- Bangalore S, Sharma A, Slotwiner A, Yatskar L, Harari R, Shah B, et al. ST-seg- ment elevation in patients with covid-19 — a case series. N Engl J Med 2020;382:2478–80.
- Modin D, Claggett B, Sindet-Pedersen C, Lassen MCH, Skaarup KG, Jensen JUS, et al. Acute COVID-19 and the incidence of ischemic stroke and acute myocar- dial infarction. Circulation 2020;142:2080–2.
- Katsoularis I, Fonseca-Rodríguez O, Farrington P, Lindmark K, Fors Con- nolly A-M. Risk of acute myocardial infarction and ischaemic stroke following COVID-19 in Sweden: a self-controlled case series and matched cohort study. Lancet 2021;398:599–607.
- Corrales-Medina VF, Madjid M, Musher DM. Role of acute infection in trig- gering acute coronary syndromes. Lancet Infect Dis 2010;10:83–92.
- Clayton TC, Thompson M, Meade TW. Recent respiratory infection and risk of cardiovascular disease: case-control study through a general practice database. Eur Heart J 2007;29:96–103.
- Musher DM, Rueda AM, Kaka AS, Mapara SM. The association be- tween pneumococcal pneumonia and acute cardiac events. Clin Infect Dis 2007;45:158–65.
- Meier CR, Jick SS, Derby LE, Vasilakis C, Jick H, Meier C, et al. Acute respira- tory-tract infections and risk of first-time acute myocardial infarction. Lancet 1998;351:1467–71.
- Barnes M, Heywood AE, Mahimbo A, Rahman B, Newall AT, Macintyre CR. Acute myocardial infarction and influenza: a meta-analysis of case–control studies. Heart 2015;101:1738–47.
- Blasco A, Coronado M-J, Hernández-Terciado F, Martín P, Royuela A, Ramil E, et al. Assessment of neutrophil extracellular traps in coronary thrombus of a case series of patients with COVID-19 and myocardial infarction. JAMA Cardiol 2021;6:469.
- Mahmud E, Dauerman HL, Welt FGP, Messenger JC, Rao SV, Grines C, et al. Management of acute myocardial infarction during the COVID-19 pan- demic. Catheter Cardiovasc Interv 2020;96:336–45.
- Gopinathannair R, Merchant FM, Lakkireddy DR, Etheridge SP, Feigofsky S, Han JK, et al. COVID-19 and cardiac arrhythmias: a global perspective on arrhythmia characteristics and management strategies. J Interv Card Electro- physiol 2020;59:329–36.
- Coromilas EJ, Kochav S, Goldenthal I, Biviano A, Garan H, Goldbarg S, et al. Worldwide survey of COVID-19–associated arrhythmias. Circ Arrhythm Electrophysiol 2021;14:285–95.
- Chorin E, Wadhwani L, Magnani S, Dai M, Shulman E, Nadeau-Routhier C, et al. QT interval prolongation and torsade de pointes in patients with COVID-19 treated with hydroxychloroquine/azithromycin. Heart Rhythm 2020;17:1425–33.
- Lazzerini PE, Capecchi PL, Laghi-Pasini F. Systemic inflammation and arrhyth- mic risk: lessons from rheumatoid arthritis. Eur Heart J 2017;38:1717–27.
- Lazzerini PE, Laghi-Pasini F, Acampa M, Srivastava U, Bertolozzi I, Giabbani B, et al. Systemic inflammation rapidly induces reversible atrial electrical re- modeling: the role of interleukin-6–mediated changes in connexin expres- sion. J Am Heart Assoc 2019;8:e011006.
- Aviles RJ, Martin DO, Apperson-Hansen C, Houghtaling PL, Rautaharju P, Kro- nmal RA, et al. Inflammation as a risk factor for atrial fibrillation. Circulation 2003;108:3006–10.
- Bhatla A, Mayer MM, Adusumalli S, Hyman MC, Oh E, Tierney A, et al. COVID-19 and cardiac arrhythmias. Heart Rhythm 2020;17:1439–44.
- Guo T, Fan Y, Chen M, Wu X, Zhang L, He T, et al. Cardiovascular implications of fatal outcomes of patients with coronavirus disease 2019 (COVID-19). JAMA Cardiol 2020;5:811.
- Amir M, Djaharuddin I, Sudharsono A, Ramadany S. COVID-19 concomitant with infective endocarditis: a case report and review of management. Int J Infect Dis 2020;98:109–12.
- Kumar R, Kumar J, Daly C, Edroos SA. Acute pericarditis as a primary presen- tation of COVID-19. BMJ Case Rep 2020;13:e237617.
- Deng Q, Hu B, Zhang Y, Wang H, Zhou X, Hu W, et al. Suspected myocardial injury in patients with COVID-19: evidence from front-line clinical observa- tion in Wuhan, China. Int J Cardiol 2020;311:116–21.
- Wang D, Hu B, Hu C, Zhu F, Liu X, Zhang J, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus–infected pneumonia in Wuhan, China. JAMA 2020;323:1061.
- Lombardi CM, Carubelli V, Iorio A, Inciardi RM, Bellasi A, Canale C, et al. Asso- ciation of troponin levels with mortality in Italian patients hospitalized with coronavirus disease 2019. JAMA Cardiol 2020;5:1274.
- Lala A, Johnson KW, Januzzi JL, Russak AJ, Paranjpe I, Richter F, et al. Preva- lence and impact of myocardial injury in patients hospitalized with COVID-19 Infection. J Am Coll Cardiol 2020;76:533–46.
- Frencken JF, van Baal L, Kappen TH, Donker DW, Horn J, van der Poll T, et al. Myocardial injury in critically ill patients with community-acquired pneumonia. a cohort study. Ann Am Thorac Soc 2019;16:606–12.
- Gao C, Wang Y, Gu X, Shen X, Zhou D, Zhou S, et al. Association between cardiac injury and mortality in hospitalized patients infected with avian influenza A (H7N9) virus. Crit Care Med 2020;48:451–8.
- Spies C, Haude V, Fitzner R, Schröder K, Overbeck M, Runkel N, et al. Serum cardiac troponin T as a prognostic marker in early sepsis. Chest 1998;113:1055–63.
- Vasile VC, Chai H-S, Khambatta S, Afessa B, Jaffe AS. Significance of elevated cardiac troponin T levels in critically ill patients with acute respiratory disease. Am J Med 2010;123:1049–58.
- Sharma A, Garcia G, Wang Y, Plummer JT, Morizono K, Arumugaswami V, et al. Human iPSC-derived cardiomyocytes are susceptible to SARS-CoV-2 infection. Cell Rep Med 2020;1:100052.
- Bojkova D, Wagner JUG, Shumliakivska M, Aslan GS, Saleem U, Hansen A, et al. SARS-CoV-2 infects and induces cytotoxic effects in human cardiomyocytes. Cardiovasc Res 2020;116:2207–15.
- Lindner D, Fitzek A, Bräuninger H, Aleshcheva G, Edler C, Meissner K, et al. Association of cardiac infection with SARS-CoV-2 in confirmed COVID-19 autopsy cases. JAMA Cardiol 2020;5:1281.
- Zhou F, Yu T, Du R, Fan G, Liu Y, Liu Z, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet 2020;395:1054–62.
- Caro-Codón J, Rey JR, Buño A, Iniesta AM, Rosillo SO, Castrejon-Castrejon S, et al. Characterization of NT-proBNP in a large cohort of COVID-19 patients. Eur J Heart Fail 2021;23:456–64.
- Carfì A, Bernabei R, Landi F. Persistent symptoms in patients after acute COVID-19. JAMA 2020;324:603.
- Daniels CJ, Rajpal S, Greenshields JT, Rosenthal GL, Chung EH, Terrin M, et al. Prevalence of clinical and subclinical myocarditis in competitive athletes with recent SARS-CoV-2 infection. JAMA Cardiol 2021:e212065.
- Puntmann VO, Carerj ML, Wieters I, Fahim M, Arendt C, Hoffmann J, et al. Outcomes of cardiovascular magnetic resonance imaging in patients recently recovered from coronavirus disease 2019 (COVID-19). JAMA Cardiol 2020;5:1265–73.
- Kotecha T, Knight DS, Razvi Y, Kumar K, Vimalesvaran K, Thornton G, et al. Patterns of myocardial injury in recovered troponin-positive COVID-19 patients assessed by cardiovascular magnetic resonance. Eur Heart J 2021;42:1866–78.
- Hayama H, Ide S, Moroi M, Kitami Y, Bekki N, Kubota S, et al. Elevated high-sensitivity troponin is associated with subclinical cardiac dysfunction in patients recovered from coronavirus disease 2019. Glob Health Med 2021;3:95–101.
- Metlay JP, Fine MJ, Schulz R, Marrie TJ, Coley CM, Kapoor WN, et al. Mea- suring symptomatic and functional recovery in patients with community-ac- quired pneumonia. J Gen Intern Med 1997;12:423–30.
- Corrales-Medina VF, Alvarez KN, Weissfeld LA, Angus DC, Chirinos JA, Chang C-CH, et al. Association between hospitalization for pneumonia and subsequent risk of cardiovascular disease. JAMA 2015;313:264.
- Jeffery MM, D’Onofrio G, Paek H, Platts-Mills TF, Soares WE, Hoppe JA, et al. Trends in emergency department visits and hospital admissions in health care systems in 5 states in the first months of the COVID-19 pandemic in the US. JAMA Intern Med 2020;180:1328–33.
- Maringe C, Spicer J, Morris M, Purushotham A, Nolte E, Sullivan R, et al. The impact of the COVID-19 pandemic on cancer deaths due to delays in diag- nosis in England, UK: a national, population-based, modelling study. Lancet Oncol 2020;21:1023–34.
- Metzler B, Siostrzonek P, Binder RK, Bauer A, Reinstadler SJ. Decline of acute coronary syndrome admissions in Austria since the outbreak of COVID-19: the pandemic response causes cardiac collateral damage. Eur Heart J 2020;41:1852–3.
- Garcia S, Albaghdadi MS, Meraj PM, Schmidt C, Garberich R, Jaffer FA, et al. Reduction in ST-segment elevation cardiac catheterization laboratory activations in the United States during COVID-19 pandemic. J Am Coll Car- diol 2020;75:2871–2.
- Mafham MM, Spata E, Goldacre R, Gair D, Curnow P, Bray M, et al. COVID-19 pandemic and admission rates for and management of acute coronary syn- dromes in England. Lancet 2020;396:381–9.
- De Filippo O, D’Ascenzo F, Angelini F, Bocchino PP, Conrotto F, Saglietto A, et al. Reduced rate of hospital admissions for ACS during Covid-19 outbreak in northern Italy. N Engl J Med 2020;383:88–9.
- Wadhera RK, Shen C, Gondi S, Chen S, Kazi DS, Yeh RW. Cardiovascular deaths during the COVID-19 pandemic in the United States. J Am Coll Car- diol 2021;77:159–69.
- Wu J, Mamas MA, MO Mohamed, Kwok CS, Roebuck C, Humberstone B, et al. Place and causes of acute cardiovascular mortality during the COVID-19 pandemic. Heart 2021;107:113–19.
- Aktaa S, Wu J, Nadarajah R, Rashid M, de Belder M, Deanfield J, et al. Inci- dence and mortality due to thromboembolic events during the COVID-19 pan- demic:multi-sourced population-based health records cohort study. Thromb Res 2021;202:17–23.
- Dunstan DW, Dogra S, Carter SE, Owen N. Sit less and move more for car- diovascular health: emerging insights and opportunities. Nat Rev Cardiol 2021;18:637–48.
- Qian C, Lyu X, Zhu H-D, Zhang Y, Du R-J, Li R, et al. Venous thromboembolism in non-COVID-19 population during the pandemic: a nationwide multicenter retrospective survey. J Thromb Thrombolysis 2021:1–7.
- Tomidokoro D, Hayama H, Okazaki T, Hara H, Hiroi Y. The effect of the COVID- 19 pandemic on incidence and characteristics of pulmonary embolism. Glob Health Med 2021;3:122–4. doi:10.35772/ghm.2020.01119.
- Silva B, Rodrigues T, Cunha N, Brito J, Alves Da Silva P, Silverio Antonio P, et al. Pulmonary embolism during the COVID-19 pandemic. Eur J Preventive Cardiol 2021;28 zwab061.183.
- Sallis R, Young DR, Tartof SY, Sallis JF, Sall J, Li Q, et al. Physical inactivity is associated with a higher risk for severe COVID-19 outcomes: a study in 48440 adult patients. Br J Sports Med 2021:bjsports-2021-104080.
- Lee SW, Lee J, Moon SY, Jin HY, Yang JM, Ogino S, et al. Physical activity and the risk of SARS-CoV-2 infection, severe COVID-19 illness and COVID-19 related mortality in South Korea: a nationwide cohort study. Br J Sports Med 2021:bjsports-2021-104203.
- Lau D, McAlister FA. Implications of the COVID-19 pandemic for cardiovascular disease and risk-factor management. Can J Cardiol 2021;37:722–32.
- Wosik J, Clowse MEB, Overton R, Adagarla B, Economou-Zavlanos N, Cavalier J, et al. Impact of the COVID-19 pandemic on patterns of outpatient cardiovascular care. Am Heart J 2021;231:1–5.
- Avaldi VM, Lenzi J, Urbinati S, Molinazzi D, Descovich C, Campagna A, et al. Effect of cardiologist care on 6-month outcomes in patients discharged with heart failure: results from an observational study based on administra- tive data. BMJ Open 2017;7:e018243.
- Hawkins NM, Scheuermeyer FX, Youngson E, Sandhu RK, Ezekowitz JA, Kaul P, et al. Impact of cardiology follow-up care on treatment and outcomes of pa- tients with new atrial fibrillation discharged from the emergency department. EP Europace 2020;22:695–703.
- Laoutaris ID, Dritsas A, Adamopoulos S. Cardiovascular rehabilitation in the COVID-19 era: ‘a phoenix arising from the ashes? Eur J Prev Cardiol 2021:zwab116.
- Eberly LA, Khatana SAM, Nathan AS, Snider C, Julien HM, Deleener ME, et al. Telemedicine outpatient cardiovascular care during the COVID-19 pan- demic. Circulation 2020;142:510–12.
- Pouwels KB, Pritchard E, Matthews PC, Stoesser N, Eyre DW, Vihta K-D, et al. Impact of Delta on viral burden and vaccine effectiveness against new SARS-CoV-2 infections in the UK. medRxiv 2021:2021.08.18.21262237.
- Rauch S, Jasny E, Schmidt KE, Petsch B. New vaccine technologies to combat outbreak situations. Front Immunol 2018;9:1963.
- US Department of Health and Human Services/Centers for Disease Control and PreventionUse of mRNA COVID-19 vaccine after reports of myocarditis among vaccine recipients: Update from the Advisory Committee on Immu- nization Practices — United States, June 2021. MMWR 2021;70:977–82.
- Kim HW, Jenista ER, Wendell DC, Azevedo CF, Campbell MJ, Darty SN, et al. Patients with acute myocarditis following mRNA COVID-19 vaccination. JAMA Cardiol 2021;27710:1–6.
- Montgomery J, Ryan M, Engler R, Hoffman D, McClenathan B, Collins L, et al. Myocarditis following immunization with mRNA COVID-19 vaccines in members of the US military. JAMA Cardiol 2021;92134:6–10.
- Utkarsh K, Lavina D, Devyani C, Ashraf SH, Alexandra BY, Annete A, et al. mRNA Coronavirus-19 Vaccine-Associated Myopericarditis in Adolescents: A Survey Study. J Pediatr 2021. doi:10.1016/j.jpeds.2021.12.025.
- Makris M, Pavord S, Lester W, Scully M, Hunt B. Vaccine-induced im- mune thrombocytopenia and thrombosis (VITT). Res PracticeThromb Haemost 2021;5:2–5.
- Pavord S, Scully M, Hunt BJ, Lester W, Bagot C, Craven B, et al. Clinical fea- tures of vaccine-induced immune thrombocytopenia and thrombosis. N Engl J Med 2021. doi:10.1056/NEJMoa2109908.
- Thaler J, Ay C, Gleixner KV, Hauswirth AW, Cacioppo F, Grafeneder J, et al. Successful treatment of vaccine-induced prothrombotic immune throm- bocytopenia (VIPIT). J Thrombo Haemostas 2021;19:1819–22.
- WHO. Guidance for clinical case management of thrombosis with thrombo- cytopenia syndrome(TTS) following vaccination to prevent coronavirus dis- ease (COVID-19). 2021. Available from: https://www.who.int/publications/i/ item/WHO- 2019- nCoV- TTS- 2021.1.
- Patriquin CJ, Laroche V, Selby R, Pendergrast J, Barth D, Côté B, et al. Thera- peutic plasma exchange in vaccine-induced immune thrombotic thrombocy- topenia. N Engl J Med 2021;385:857–9.
- Barda N, Dagan N, Ben-Shlomo Y, Kepten E, Waxman J, Ohana R, et al. Safety of the BNT162b2 mRNA Covid-19 vaccine in a nationwide setting. N Engl J Med 2021:NEJMoa2110475.
- Hippisley-Cox J, Patone M, Mei XW, Saatci D, Dixon S, Khunti K, et al. Risk of thrombocytopenia and thromboembolism after covid-19 vaccination and SARS-CoV-2 positive testing: self-controlled case series study. BMJ 2021;374:n1931.