注:この記事は、有識者個人の意見です。COVID-19有識者会議の見解ではないことに留意ください。
- 新型コロナウイルスの変異に伴って従来の治療の有効性が低下することがあるため、さまざまな治療法の多角的な研究を継続する必要がある。
- COVID-19の回復者の抗体価は個人差が大きい。回復者血漿の研究を進める中で、対象者や研究参加機関の負担を減らすためには、抗体価が高い対象者から血漿を採取することが重要である。そのような対象者の背景を明らかにするために、本研究を実施した。
- この研究では、COVID-19の回復者血漿研究の参加者を対象とした。採取した血液検体を利用して、新型コロナウイルスのS蛋白に対するIgG抗体を測定し、高い抗体価を示す回復者の背景を検討した。
- 581人の参加者のうち、必要な情報をすべて確認できた534人を解析の対象とした。重回帰分析の結果、年齢が高いこと、発症から血漿採取までの日数が短いこと、COVID-19発症時に発熱があったこと、COVID-19の治療として副腎皮質ステロイドの全身投与を受けたこと、そして血液型がAB型であることが高い抗体価と関係していることが判明した。
- COVID-19の回復者血漿採取における候補者として上記の背景を有する回復者が望ましい。これらの条件を回復者血漿採取の基準に組み入れることによって、適切な回復者からの血漿採取が可能となることが期待できる。
はじめに
COVID-19の世界的な流行以後、すでにさまざまな治療法が研究され、現在も新たな治療法の研究開発が続けられている。回復者血漿を用いた治療についても世界的に研究されていたが、多くの研究ではその有効性を示すことができず、世界保健機関(WHO)は2021年12月7日付のガイドライン[1]において、COVID-19の治療として回復者血漿を使用しないことを推奨している。ただし、高齢かつ重症の患者や、発症から非常に早期の患者を対象に高力価の回復者血漿製剤を投与すると、回復者血漿が有効だったという研究結果も報告されている[2,3]。さらに、オミクロン変異株に対して、抗体製剤(カシリビマブ/イムデビマブ)の効果が低下していることを示す報告もある[4,5]。今後もウイルスの変異によってそれまでの治療法の効果が低下する可能性があることから、さまざまな治療法を多角的に研究しつづける必要がある。
回復者血漿を用いたさまざまな研究においては、COVID-19から回復した対象者から抗体を含む血漿を採取する必要がある。COVID-19の抗体価は、軽症患者よりも重症患者で高いと報告されているが[6]、時間とともに減少することがわかっており、ピークに達した後の半減期は約40日と報告されている[7,8]。抗体価の低い対象者から血漿を採取することは、本人および研究参加機関の双方に負担をかけることになる。抗体価の高い対象者を予測することができれば、回復期血漿提供のためのスクリーニングを効率的に行うことができる。本研究では、回復期血漿採取に参加した対象者のデータを分析することにより、COVID-19の回復者の日本人において、抗体価が高い背景因子を明らかにすることを目的とした。
方法
国立国際医療研究センターで実施されたCOVID-19の回復者血漿研究[9]に2020年4月30日から2021年4月8日までに参加した方を対象とした。この回復者血漿研究の参加者は、COVID-19の発症から3週間以上が経過し、かつ20-69歳までに限定されていた。初日にCOVID-19の発症日、経過、症状、診断日、入院の有無、治療内容などに関する自己回答形式の質問票を記入してもらい、研究の参加条件を満たしていることを確認後、血液型検査と抗体価測定のための採血を行った。今回の研究では、このときのS蛋白に対するIgG抗体の測定結果を使用して解析した。
連続変数は中央値および四分位範囲(IQR)で示し、カテゴリー変数は症例数および割合で示した。高い抗体価を示す対象者の背景因子を特定するために、重回帰分析を行った。重回帰分析に用いる変数は著者らのグループによる検討の結果、臨床的に重要と思われる因子(年齢、性別、発症から検体採取までの日数、COVID-19発症時の発熱、人工呼吸器の有無、COVID-19の治療として副腎皮質ステロイドの全身投与を受けたこと、高血圧、糖尿病、血液型がAB型であること)を選択した。
結果
研究対象者586名のうち、抗体価が測定できなかった5名を除く581名の背景を【表1】に示す。年齢の中央値は46(IQR:38-54)歳、49.4%が男性、9.9%が血液型AB型だった。COVID-19発症時の症状として多かったのは発熱(84.2%)、咳(42.9%)だった。全体の54.8%が入院したが、全体の84.5%は酸素投与を必要としなかった。発症から抗体価測定用の検体採取までの日数の中央値は63(IQR:38-102)日、抗体価の中央値は33.7(IQR:13.2-73.3)AU/mLであった。なお,採取時にCOVID-19のワクチン接種歴がある者はいなかった。
| 表1 |
| 参加者の背景 (n=581) |
| a欠損値のため、項目毎に分母は異なるb無症候だった12名においては、陽性となった検体の採取日を発症日と扱った |
 |
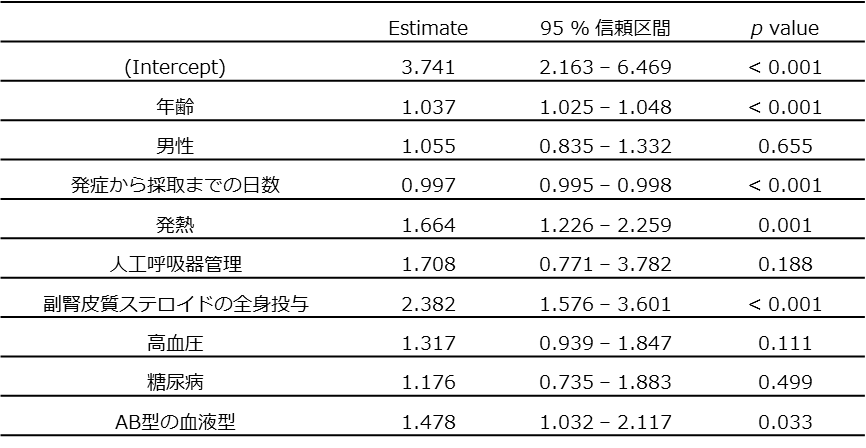
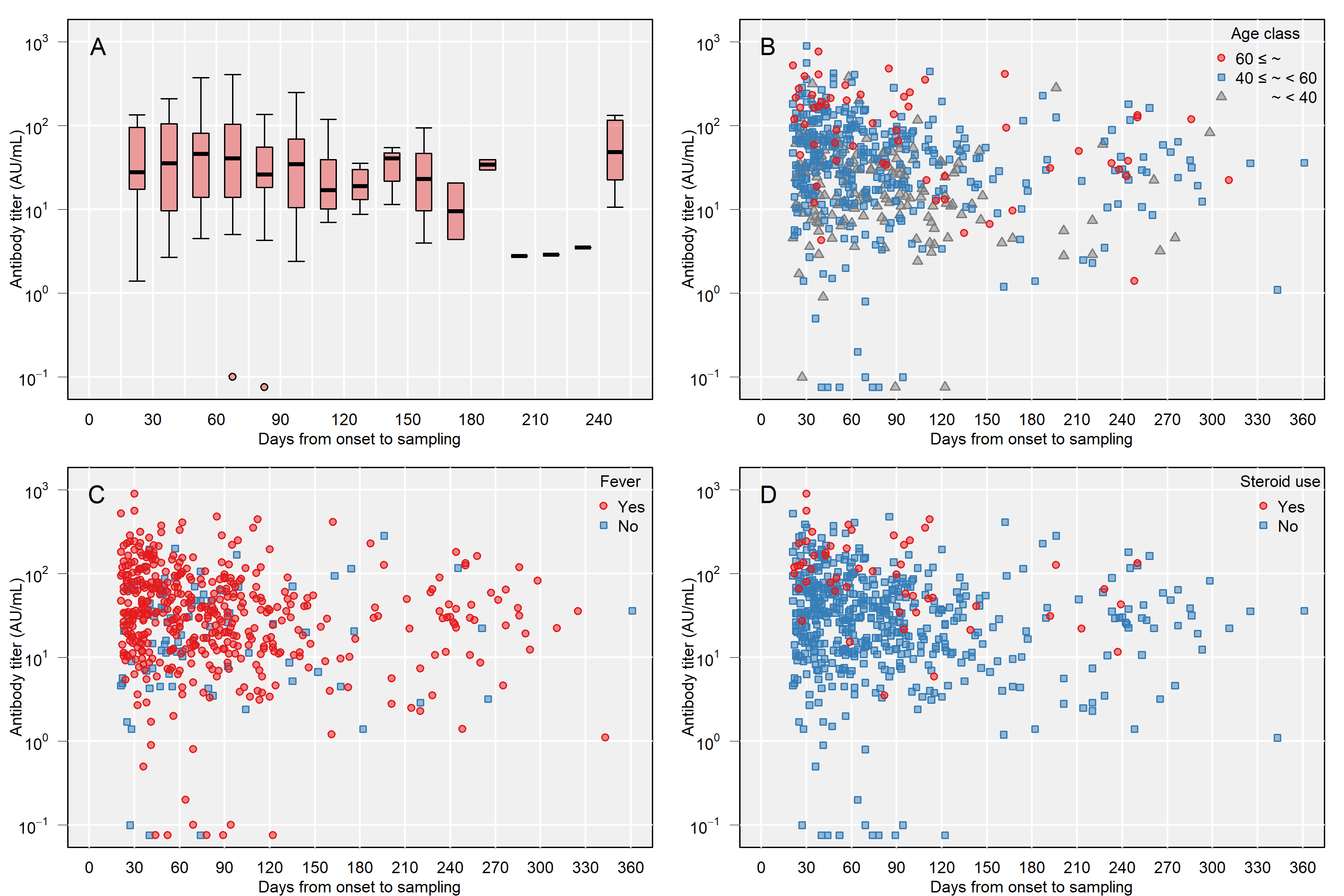
必要な情報がすべてそろっている534人の参加者を対象として、重回帰分析を行った。独立変数に応じた抗体価上昇量の推定値を【表2】に示す。年齢が高いこと、発症から血漿採取までの日数が短いこと、COVID-19発症時に発熱があったこと、COVID-19の治療として副腎皮質ステロイドの全身投与を受けたこと、そして血液型がAB型であることが、高い抗体価の予測の予測因子と判明した。【図1A-D】および【図2】は、これらの有意な変数について、発症からの日数と抗体価の関連を示したものである。
| 表2 |
| 重回帰分析の結果 (n=534) |
 |
| 図1 |
| 発症からの日数と抗体価の関係 |
| A:経過日数、B:年齢別、C:発症時の発熱の有無、D:副腎皮質ステロイド全身投与の有無 |
 |
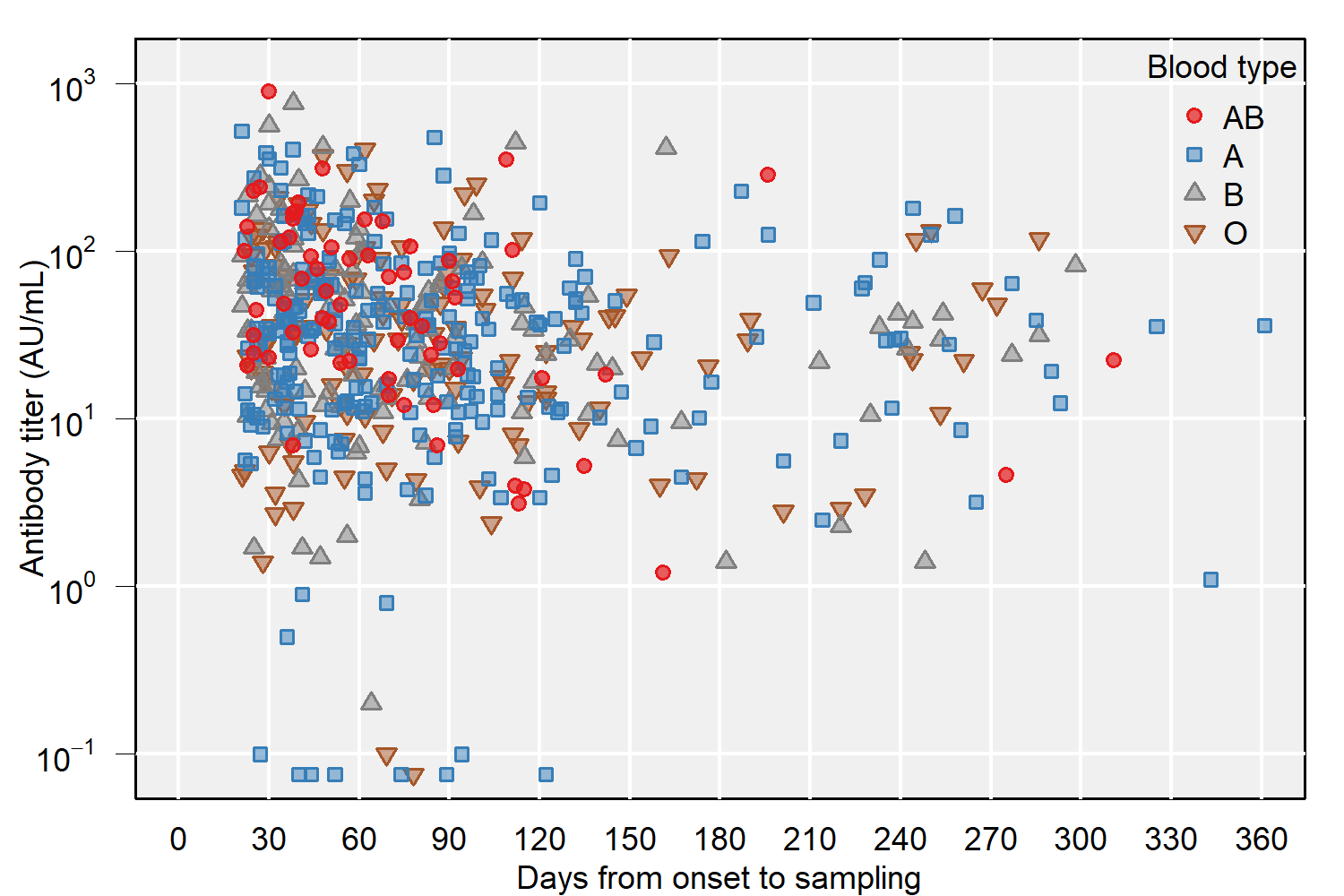
| 図2 |
| 発症からの日数と抗体価の関係 ABO式血液型別 |
 |
考察
中国の先行研究[10]では、抗体価の高さはCOVID-19発症中の発熱の有無と関係していたものの、年齢、性別、ABO血液型とは相関がないことが示されている。ドイツの先行研究[11]では、COVID-19発症中の発熱のほかに、入院の有無も抗体価と関連があったと報告されている。一方、今回の研究ではCOVID-19の治療として副腎皮質ステロイドの全身投与を受けた患者では抗体価が高いことがわかった。この知見は先行研究[10-12]では言及されていない。一般的に副腎皮質ステロイド製剤は免疫反応を抑制する作用があるが、RECOVERY研究[13]の結果を受けて、現在では酸素投与を要するCOVID-19患者に対してデキサメタゾンなどの副腎皮質ステロイドを投与することが一般的となっている。つまり、本研究の結果は、副腎皮質ステロイドの全身投与を必要とするほど重症の患者では、回復後の抗体価が高いことを示唆していると思われる。本質的には、重症患者において抗体価が高い傾向にあることを表しているのかもしれない。
また、本研究では発症から血漿採取までの日数が短いと抗体価が高いことがわかった。中和抗体が時間とともに低下する[7]ことはすでに報告されており、回復者血漿採取においても、できるだけ発症から早い時期に血漿を採取することが望ましい。回復者血漿採取のスクリーニング基準に、発症からの日数を追加することは合理的だろう。また、時間経過とともに抗体価が下がってしまうことから、継続的に新しい参加者を募集する必要があると思われる。
今回の研究でもう一つ注目すべき点は、血液型がAB型の参加者の抗体価が他の血液型の参加者よりも高かった点である。日本人の約10%がAB型と推定されており[14]、本研究でも参加者全体でAB型の割合は同程度だった。先行研究では、AB型のドナーはO型のドナーよりも抗体価が高く[15,16]、COVID-19感染者は非感染者よりもABO抗体が低いと報告されている[17]。これらの知見は、ABO式血液型がCOVID-19の感染や抗体産生に何らかの影響を及ぼしている可能性を示している。血液型がAB型の対象者から採取した血漿は、理論的にはどの血液型の患者にも提供できることから、血液型がAB型の人には回復者血漿採取への参加を前向きに検討してもらうほうがいいだろう。
一方、今回の研究では、人工呼吸器の使用の有無と抗体価の高さについて、統計学的に有意な結果は得られなかった。人工呼吸器管理を受けた場合、副腎皮質ステロイドの使用期間がより長く、使用量がより多い可能性がある。また、トシリズマブやバリシチニブといったさまざまな免疫抑制薬が使用されることが多い。そのような薬剤の使用歴が、今回の結果に影響を与えた可能性があると考える。
おわりに
今回の研究では、年齢が高いこと、発症から血漿採取までの日数が短いこと、COVID-19発症時に発熱があったこと、COVID-19の治療として副腎皮質ステロイドの全身投与を受けたこと、そして血液型がAB型であることが高い抗体価と関係していることが判明した。抗体価が高い対象者を集中的に募集するためには、これらの背景を参考にすることが望ましい。今後はCOVID-19の回復後にワクチン接種を受けた対象者における抗体産生の程度や傾向を明らかにする研究も必要である。
[引用文献]
- World Health Organization, Therapeutics and COVID-19. Accessed Dec 27, 2021.
https://www.who.int/publications/i/item/WHO-2019-nCoV-therapeutics-2021.4 - Libster R, Pérez Marc G, Wappner D, Coviello S, Bianchi A, Braem V, et al. Early High-Titer Plasma Therapy to Prevent Severe Covid-19 in Older Adults. N Engl J Med. 2021;384:610-618. doi: 10.1056/NEJMoa2033700.
- David J. Sullivan, Kelly A. Gebo, Shmuel Shoham, Evan M. Bloch, Bryan Lau, Aarthi G. Shenoy, et al. Randomized Controlled Trial of Early Outpatient COVID-19 Treatment with High-Titer Convalescent Plasma. medRxiv 2021.12.10.21267485; doi: https://doi.org/10.1101/2021.12.10.21267485
- Alexander Wilhelm, Marek Widera, Katharina Grikscheit, Tuna Toptan, Barbara Schenk, Christiane Pallas, et al. Reduced Neutralization of SARS-CoV-2 Omicron Variant by Vaccine Sera and Monoclonal Antibodies. medRxiv 2021.12.07.21267432; doi: https://doi.org/10.1101/2021.12.07.21267432
- Nariko Ikemura, Atsushi Hoshino, Yusuke Higuchi, Shunta Taminishi, Tohru Inaba, Satoaki Matoba. SARS-CoV-2 Omicron variant escapes neutralization by vaccinated and convalescent sera and therapeutic monoclonal antibodies. medRxiv 2021.12.13.21267761; doi: https://doi.org/10.1101/2021.12.13.21267761
- Kutsuna S, Asai Y, Matsunaga A. Loss of anti-SARS-CoV-2 antibodies in mild Covid-19. N Engl J Med 2020;383:1695–6. https://doi.org/ 10.1056/NEJMc2027051.
- Gontu A, Srinivasan S, Salazar E, Nair MS, Nissly RH, Greenawalt D, et al. Limited window for donation of convalescent plasma with high live-virus neutralizing antibody titers for COVID-19 immunotherapy. Commun Biol 2021;4:267. https://doi.org/10.1038/s42003-021-01813-y.
- Yamayoshi S, Yasuhara A, Ito M, Akasaka O, Nakamura M, Nakachi I, et al. Antibody titers against SARS-CoV-2 decline, but do not disappear for several months. EClinicalMedicine 2021;32:100734. https://doi.org/10.1016/j.eclinm.2021.100734.
- Terada M, Kutsuna S, Togano T, Saito S, Kinoshita N, Shimanishi Y, et al. How we secured a COVID-19 convalescent plasma procurement scheme in Japan. Transfusion. 2021;61:1998-2007. https://doi.org/10.1111/trf.16541.
- Li L, Tong X, Chen H, He R, Lv Q, Yang R, et al. Characteristics and serological patterns of COVID-19 convalescent plasma donors: optimal donors and timing of donation. Transfusion 2020;60:1765–72. https://doi.org/10.1111/trf.15918.
- Schlickeiser S, Schwarz T, Steiner S, Wittke K, Al Besher N, Meyer O, et al. Disease severity, fever, age, and sex correlate with SARS-CoV-2 neutralizing antibody responses. Front Immunol 2021;11:628971. https://doi.org/10.3389/fimmu.2020.628971.
- Benner SE, Patel EU, Laeyendecker O, Pekosz A, Littlefield K, Eby Y, et al. SARS-CoV-2 antibody avidity responses in COVID-19 patients and convalescent plasma donors. J Infect Dis 2020;222:1974–84. https://doi.org/10.1093/infdis/jiaa581.
- RECOVERY Collaborative Group, Horby P, Lim WS, Emberson JR, Mafham M, Bell JL, Linsell L, et al. Dexamethasone in hospitalized patients with Covid-19. N Engl J Med 2021;384:693–704. https://doi.org/10.1056/NEJMoa2021436.
- Fujita Y, Tanimura M, Tanaka K. The distribution of the ABO blood groups in Japan. Jinrui Idengaku Zasshi 1978;23:63–109. https://doi.org/10.1007/BF02001790.
- Madariaga MLL, Guthmiller JJ, Schrantz S, Jansen MO, Christensen C, Kumar M, et al. Clinical predictors of donor antibody titre and correlation with recipient antibody response in a COVID-19 convalescent plasma clinical trial. J Intern Med 2021;289:559–73. https://doi.org/10.1111/joim.13185.
- Hayes C, Rubenstein W, Gibb D, Klapper E, Tanaka J, Pepkowitz S. Blood group O convalescent plasma donations have significantly lower levels of SARS-CoV-2 IgG antibodies compared to blood group A donations. Transfusion. 2021;61:2245-2249. doi: 10.1111/trf.16524.
- Deleers M, Breiman A, Daubie V, Maggetto C, Barreau T, Besse T, et al. Covid-19 and blood groups: ABO antibody levels may also matter. Int J Infect Dis 2021;104:242–9. https://doi.org/10.1016/j.ijid.2020.12.025.