- SARS-CoV-2によるパンデミックが大きな被害をもたらす中、世界各国でCOVID-19ワクチンの接種が進んでいる。日本でも複数のワクチンが特例承認され、感染の収束が期待されている。
- 国内におけるSARS-CoV-2変異株の感染が多数報告され、ワクチン効果の低下が懸念されている。
- 特に、ベータ(B.1.351)、ついでデルタ(B.1.617.2)変異ウイルスはワクチン効果を低下させることが示唆されている。
- 各ワクチン開発会社は、変異株向けの改変型ワクチンの開発に着手し、有望な結果が報告されている。
- 国産ワクチンの開発も進んでおり、早期に承認されることが望まれる。
COVID-19ワクチンの開発
2019年の終わりに、中国で新型コロナウイルスSevere Acute Respiratory Syndrome coronavirus 2(SARS-CoV-2)が流行を起こしてから約1年半が経過した。新型コロナウイルスは、今もなお世界中で猛威をふるい、甚大な健康被害ならびに経済被害をもたらし続けている。一方で、前例のないスピードでワクチンの開発と実用化が進み、一部の国ではワクチン接種による感染抑止効果が確認されている。現在、日本国内で承認申請されているワクチンおよび特例承認されているワクチンを以下に挙げる【図表1】。
| 図表1 |
| 接種が進んでいる主なCOVID-19ワクチン |
| 有効性は試験ごとに多少異なるが、代表的な値を示した。 |
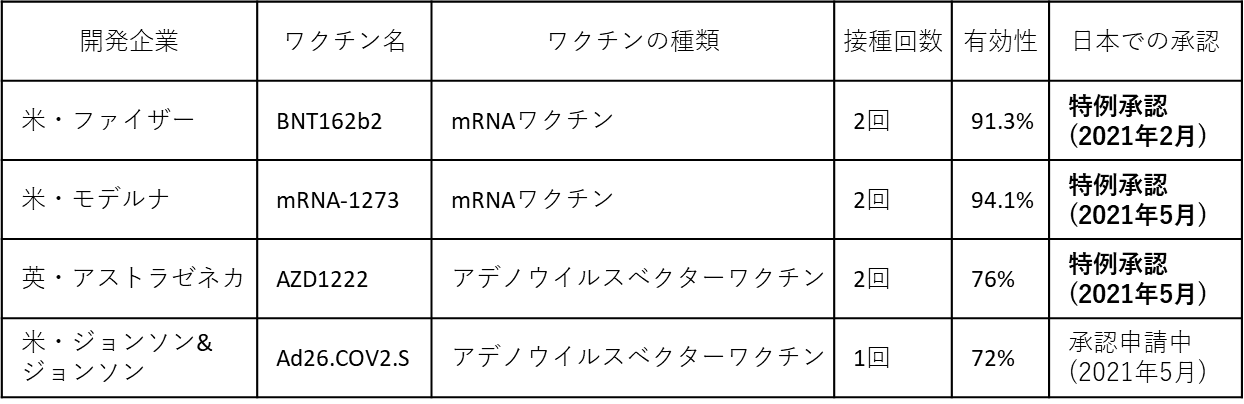 |
ファイザー社のBNT162b2(商品名:コミナティ)は、SARS-CoV-2のスパイク蛋白質を発現させるためのmRNAを用いたワクチンである。日本でも2021年2月にCOVID-19ワクチンとして最も早く特例承認され、医療従事者や高齢者を中心に接種が進んでいる。モデルナ社のmRNA-1273(商品名:COVID-19ワクチンモデルナ)もmRNAワクチンである。日本では5月に特例承認され、東京と大阪の大規模接種会場で接種が実施されている。mRNAワクチンは新しいタイプのワクチンであり、COVID-19のパンデミック以前に承認されたものはなかったが、BNT162b2およびmRNA-1273はともに2回の接種後の有効性が90%以上という非常に高い効果が報告されている[1,2]。
現在、日本で特例承認されている3つ目のワクチンがアストラゼネカ社のAZD1222(商品名:バキスゼブリア)である。これは、チンパンジーを由来とするアデノウイルスベクターにSARS-CoV-2のスパイク遺伝子を組み込んだワクチンである。長期保存には-20℃以下での保冷が必須なmRNAワクチンよりも安定で、4℃での長期保存が可能という利点がある。しかしながら、極めて稀ではあるものの、ワクチン接種後の血栓症の発症が報告されており、一部の国では接種が中断された。日本でも5月に特例承認されたが、実際の接種予定は明らかとなっていない。
ジョンソン&ジョンソン社のAd26.COV2.Sもスパイク遺伝子を組み込んだアデノウイルスベクターワクチンである。前述の3種類のワクチンは2回接種が必要である一方、Ad26.COV2.Sは1回のみの接種で良いという特徴がある。日本では承認申請中であるものの、これまでの使用実績からアストラゼネカ社のワクチン同様に、稀なワクチン接種後の血栓症が問題となっている。これを受けて、アメリカでは一時的に接種の中断が勧告されたが、血栓症は極めて稀であり、ワクチン接種による利益が血栓症のリスクを上回るとして接種が再開されている。アデノウイルスベクターワクチンは、mRNAワクチンと比べると有効性が若干劣るものの、概ね70%程度の有効性が期待できる[3–5]。
変異株の出現とワクチンの効果
SARS-CoV-2変異株の出現
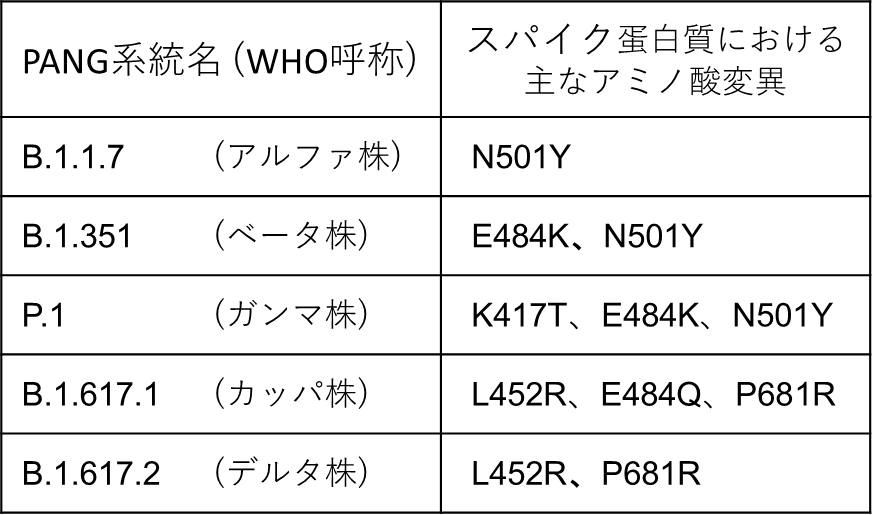
ワクチン接種によりパンデミック収束への期待が高まる中、スパイク蛋白質の抗原決定基にアミノ酸変異を有する変異株の出現が世界各地で報告されている。日本でも、海外から流入した変異株の感染が相次いで報告されており、変異株の蔓延や置き換わりが進んでいる。SARS-CoV-2はウイルスゲノムに塩基変異が生じることが多いRNAウイルスであるため、変異株が新たに発生しないかを常に注視していく必要がある。現在注目されている主な変異株を以下に挙げる。WHOが5月31日に発表した新たな命名システムによって、主な変異株には、B.1.1.7などの科学的な分類に従った名称の他に、アルファ、ベータといったギリシャ文字を使った呼称が割り当てられることとなった【図表2】。
| 図表2 |
| 主なSARS-CoV-2変異株 |
 |
変異株に対するワクチンの有効性
変異株の出現に際し、感染性や病原性の変化と同時に懸念されるのが、現行のワクチンの有効性である。特例承認されたワクチンおよび開発中のワクチンのほとんどは、SARS-CoV-2のスパイク蛋白質を免疫抗原として利用している。そのため、スパイク蛋白質の抗原決定基にアミノ酸変異を持つ変異株は、ワクチン接種によって獲得された免疫から逃れ、ワクチンの有効性が低下する可能性がある。図表2の変異株に対するワクチン効果は以下の通りである。
B.1.1.7系統の変異株(アルファ株)
イギリスで最初に検出され、他国にも急速に拡大したこの変異株は、従来株よりも感染性が高まっていることが示唆されている[6,7]。病原性には大きく影響しないという報告[8,9]もあるが、重症化のリスクが高いという報告[10]もあり、引き続き警戒が必要である。一方で、mRNAワクチン接種者の血清のB.1.1.7変異株に対する中和活性は、従来株に対する中和活性と同等であった[11,12]。B.1.1.7変異株が蔓延していた地域で行われた臨床試験においても、ファイザー社のワクチンは全体として87~95.3%という高い有効性を示した[13,14]。また、アストラゼネカ社のワクチンも、B.1.1.7変異株に対して70.4%の有効性を示している[15]。これらの結果から、B.1.1.7変異株に対して既存ワクチンの有効性は低下しないと考えられる。
B.1.351系統の変異株(ベータ株)
ワクチン効果を減弱させるという報告が多数あり、ワクチン効果低下の懸念が最も高い。mRNAワクチン接種者の血清のB.1.351変異株に対する中和活性は、従来株に対する中和活性に比べ、顕著に低下していた[12]。しかし、カタールで行われた試験において、ファイザー社のワクチンはB.1.351変異株に対して72.1~75%の有効性を示した[14]。また、ジョンソン&ジョンソン社のアデノウイルスベクターワクチンも、南アフリカで行われた臨床試験では、感染例の94.5%がB.1.351変異株によるものであったが、全体として64%の有効性を示した(感染例の95%以上が従来株によるものであったアメリカにおける臨床試験での有効性は72%であった。)[4]。
一方で、アストラゼネカ社のアデノウイルスベクターワクチンは、南アフリカで行われた臨床試験において、B.1.351変異株に対する有効性が10.4%であった。被験者が2000人と比較的少数であるため結論を出すのは尚早との指摘もあるが、有効性が低下している可能性が高いと考えられる[16]。この結果を受けて、南アフリカではアストラゼネカ社のワクチンの接種が停止された。同じアデノウイルスベクターワクチンであるにも関わらず、アストラゼネカ社のワクチンとジョンソン&ジョンソン社のワクチンとでB.1.351変異株に対する有効性に差が見られる原因は明らかではない。両者の違いとしては、アストラゼネカ社はチンパンジー由来のアデノウイルスベクターを利用しており、ジョンソン&ジョンソン社はAd26というヒトのアデノウイルスベクターを利用している点が挙げられる。また、ジョンソン&ジョンソン社のワクチンがコードしているスパイク蛋白質にはフリン切断部位の変異やプレフュージョン構造を安定化する2ヶ所のプロリン変異(K986P,V987P)が導入されている。K986P,V987Pの変異はファイザー社やモデルナ社のmRNAワクチンがコードするスパイク蛋白質にも導入されているが、アストラゼネカ社のワクチンがコードするスパイク蛋白質には導入されていない。ジョンソン&ジョンソン社の前臨床試験において、従来株に対してはフリン切断部位の変異およびプロリン変異の導入によってワクチンの有効性が高まることが示されている[17]。従って、ベクターの違いやスパイク蛋白質の変異がB.1.351に対する有効性の違いに影響している可能性が考えられる。また、承認申請前の米・ノババックス社のDNAワクチンも、従来株に対する有効性が96%であったのに対し、B.1.351変異株に対する有効性は51%であった[18]。
以上のように、ファイザー社やジョンソン&ジョンソン社のワクチンは、有効性が若干低下する傾向はあるものの、B.1.351変異株に対しても一定以上の効果が期待できる。とはいうものの、有効性低下の傾向が認められるため、B.1.351変異株に対応した改変型ワクチンの開発が進んでいる(後述)。
P.1系統の変異株(ガンマ株)
P.1変異株は、従来株の感染によって獲得された免疫から一定程度逃れることができ、再感染のリスクが高まる可能性が指摘されている[19]。ブラジルのマナウスでは、2020年10月までに76%の人がSARS-CoV-2に感染し集団免疫を達成したと推定されていたにも関わらず、2021年に入って再び大規模な流行が起きた。その流行がP.1変異株により起きていたため、P.1変異株が既感染者の免疫から逃避した可能性が考えられている[20]。これが正しければ、P.1変異株は従来株向けのワクチンの接種によって獲得された免疫からも逃れられることが想定される。P.1変異株に対するワクチンの有効性に関するデータは限られているが、B.1.351変異株と同じくスパイク蛋白質にE484K変異を有することから、ワクチン効果が低下することが懸念される。mRNAワクチン接種者の血清の中和活性は、B.1.351変異株に対する中和活性が最も低いが、P.1変異株に対する中和活性もそれに次いで低かった[12]。また、ブラジルで行われた試験において、ジョンソン&ジョンソン社のアデノウイルスベクターワクチンは68.1%の効果を示した[4]。
B.1.617.1およびB.1.617.2系統の変異株(カッパ株およびデルタ株)
B.1.617.1変異株は、スパイク蛋白質にL452RおよびE484Qという2つのアミノ酸変異を持つことから日本では二重変異株とも称される。B.1.617.2変異株は、L452R変異を持つもののE484Q変異を持たない。両変異株はスパイク蛋白質にP681Rという変異も持ち、このアミノ酸変異によりウイルスの細胞への感染性が上昇していることが示唆されている。
2021年6月現在、イギリスではB.1.617.2変異株による感染例が急速に増加しており、注目が高まっている。ファイザー社またはモデルナ社のmRNAワクチンを接種した人の血清の中和活性は、L452R-E484Qの二重変異またはL452R-E484Q-P681Rの三重変異によって3~5分の1に低下し、L452RやE484Qの単独変異でも3~4分の1に低下した[21]。別の研究では、B.1.617.1変異株に対してファイザー社のワクチン接種者の血清の中和活性が3分の1に低下(B.1.351変異株に対しては11分の1に低下)したことが報告されている[22]。
また、イギリスにおいてファイザー社およびアストラゼネカ社のワクチンの有効性を調査した結果、B.1.617.2変異株に対しては効果が若干低下することが報告された[23]。ファイザー社のワクチンを2回接種した場合、B.1.1.7変異株に対する有効性は93.4%であったが、B.1.617.2変異株に対する有効性は87.9%であった。アストラゼネカ社のワクチンを2回接種した場合、B.1.1.7変異株に対する有効性は66.1%、B.1.617.2変異株に対する有効性は59.8%であった。また、2回接種後はB.1.617.2変異株に対してもある程度の効果が維持されていたが、1回のみ接種した場合はB.1.617.2変異株に対する有効性がより顕著に低下し、2回接種の重要性が明らかになっている。B.1.351変異株と比較すると、ワクチン効果の低下は小さいことが示唆されるが、感染性や病原性の情報が蓄積されるまでは引き続き注意が必要である。
ワシントン大学医学部保健指標評価研究所(Institute for Health Metrics and Evaluation、IHME)は、報告されたデータとそれらに基づいた推定値を合わせて、各ワクチンの各変異株に対する効果を以下のようにまとめている[24]【図表3】。
| 図表3 |
| 変異株に対するワクチンの効果 |
| IHMEのCOVID-19 resources(http://www.healthdata.org/covid/covid-19-vaccine-efficacy-summary) より抜粋、改変。変異株ごとのワクチンの効果を示した。数値は試験のデータに基づくもの。( )内の数値は試験データに基づいた推定値。 |
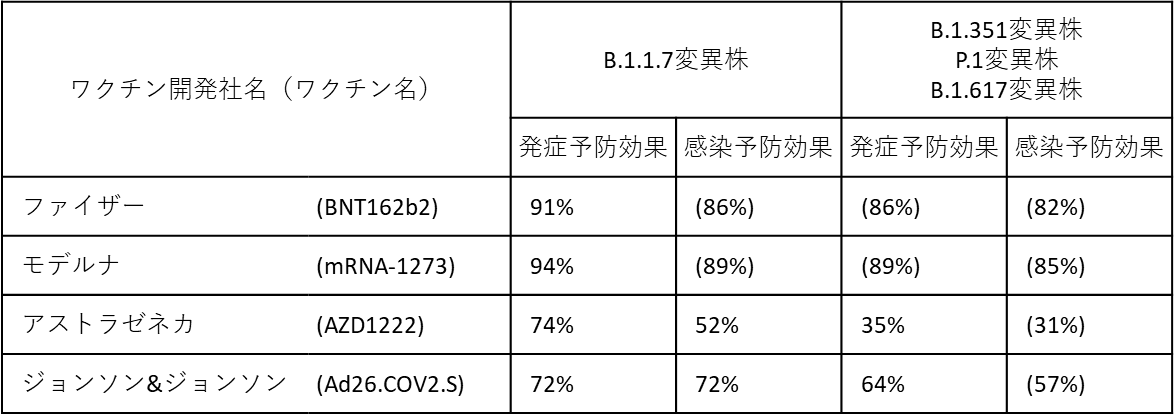 |
現在までのところ、各ワクチンの変異株に対する有効性に高低はあるものの、どの変異株に感染した場合であっても高い重症化予防効果が期待できることが示唆されている。従って、これまでに知られているどの変異株が蔓延してもワクチン接種のメリットは大きいと考えられる。
変異株を考慮した変異株対応型ワクチン開発の取り組み
変異株に対してワクチン効果が減弱する可能性があるという報告を受け、一部の企業では変異株に対応したワクチンの開発が始まっている。
モデルナ社は、B.1.351変異株に対応した改変型mRNAワクチンの開発を開始したことを2021年3月に発表した。現行のmRNA-1273は従来株のスパイク蛋白質をコードしているが、新たにB.1.351変異株のスパイク蛋白質をコードしたmRNA-1273.351を開発中である。さらに、mRNA-1273とmRNA-1273.351を混合して接種するmRNA-1273.211の試験も進めている。マウスにmRNA-1273.351またはmRNA-1273.211を2回接種すると、B.1.351変異株に対する中和抗体が誘導されていた[25]。また、mRNA-1273を2回接種したマウスにmRNA-1273.351を接種すると従来株とB.1.351変異株の両方に対して中和抗体価の上昇が認められた。現在進行中の第Ⅰ/Ⅱ相の臨床試験では、mRNA-1273を2回接種済みの被験者にmRNA-1273.351を接種したところ、従来株、B.1.351変異株およびP.1変異株に対する中和抗体価の上昇が確認された[26]。ブースターワクチンとして、2021年下期以降の供給開始が見込まれている。ファイザー社も、B.1.351変異株に対応した改変型ワクチンの開発に着手したことを2021年2月に発表した。また、アストラゼネカ社も2021年4月からB.1.351変異株向けの改変型ワクチンの開発を始めており、年内の供給開始を目指すとしている。
mRNAワクチンやアデノウイルスベクターワクチンは、これまで主流であった不活化ワクチンと比較すると変異株に対応するために変更する事項が少なくて済むという利点があり、変異株に対応するワクチンの開発も短時間で可能となることが期待される。
日本国内におけるワクチン開発
日本国内でも、複数の企業がCOVID-19ワクチン開発に取り組んでいる。主な国産ワクチンの開発状況は以下の通りである【図表4】。
| 図表4 |
| 日本で開発中のCOVID-19ワクチンとその進捗状況 |
| 2021年6月現在。 |
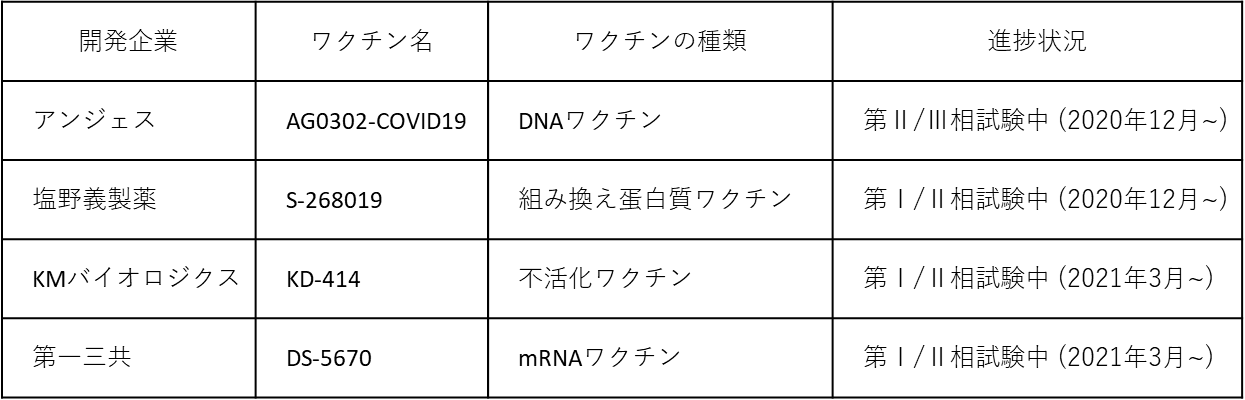 |
4社とも、現在臨床試験中となっている。海外に頼らず、有効性の高いワクチンを供給できる体制を整えておくことは重要だが、未だ承認の目処は立っていない。本来、ワクチンの承認には大規模な第Ⅲ相試験を経る必要がある。しかしながら、既に特例承認されたワクチンの接種が進んでいる現状において、プラセボ群をおいた試験の実施が倫理面で困難となっている。国産ワクチンの早期承認を可能にすべく、承認手続きの迅速化や大規模試験に代わる試験の導入など、承認制度の見直しが検討されている。塩野義製薬は、生産体制の整備も進んでおり承認条件によっては年内の供給開始が可能であるとしている。また、アンジェスと塩野義製薬は、それぞれ変異株向けのワクチン開発にも着手済みであることを発表している。
おわりに
COVID-19が甚大な被害をもたらす中、1年足らずという異例のスピードでワクチンが開発されたというのは偉大な成果であると言える。現在広く接種されているmRNAワクチンは有効性も高く、パンデミックの収束に大きく貢献することが予想される。しかしながら、変異株の出現が相次いで報告されており、引き続き警戒が必要である。変異株向けのワクチン開発も始まっているが、3回目以降の追加接種の安全性などの検証も必要であり、実用化されるまでにはまだ時間がかかると考えられる。また、従来株の感染であっても、ワクチン接種によって完全に防ぐことができるわけではないため、ワクチン接種後の感染例が報告されている。変異株の監視や解析を続けるとともに、ワクチンの効果を過信することなく基本的な感染対策の徹底を続けていく必要がある。
[引用文献]
- Baden LR, El Sahly HM, Essink B, Kotloff K, Frey S, Novak R, et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. New England Journal of Medicine. 2021 Feb;384(5):403–16.
- Polack FP, Thomas SJ, Kitchin N, Absalon J, Gurtman A, Lockhart S, et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. New England Journal of Medicine. 2020 Dec;383(27):2603–15.
- AZD1222 US Phase III primary analysis confirms safety and efficacy [Internet]. [cited 2021 Jun 6]. Available from: https://www.astrazeneca.com/media-centre/press-releases/2021/azd1222-us-phase-iii-primary-analysis-confirms-safety-and-efficacy.html
- Sadoff J, Gray G, Vandebosch A, Cárdenas V, Shukarev G, Grinsztejn B, et al. Safety and Efficacy of Single-Dose Ad26.COV2.S Vaccine against Covid-19. New England Journal of Medicine. 2021 Apr.
- Voysey M, Costa Clemens SA, Madhi SA, Weckx LY, Folegatti PM, Aley PK, et al. Single-dose administration and the influence of the timing of the booster dose on immunogenicity and efficacy of ChAdOx1 nCoV-19 (AZD1222) vaccine: a pooled analysis of four randomised trials. The Lancet. 2021 Mar;397(10277):881–91.
- Davies NG, Abbott S, Barnard RC, Jarvis CI, Kucharski AJ, Munday JD, et al. Estimated transmissibility and impact of SARS-CoV-2 lineage B.1.1.7 in England. Science. 2021 Apr 9;372(6538):eabg3055. doi: 10.1126/science.abg3055.
- Munitz A, Yechezkel M, Dickstein Y, Yamin D, Gerlic M. BNT162b2 vaccination effectively prevents the rapid rise of SARS-CoV-2 variant B.1.1.7 in high-risk populations in Israel. Cell Reports Medicine. 2021 May;2(5):100264.
- Frampton D, Rampling T, Cross A, Bailey H, Heaney J, Byott M, et al. Genomic characteristics and clinical effect of the emergent SARS-CoV-2 B.1.1.7 lineage in London, UK: a whole-genome sequencing and hospital-based cohort study. The Lancet Infectious Diseases. 2021 Apr 12;S1473-3099(21)00170-5. doi: 10.1016/S1473-3099(21)00170-5.
- Graham MS, Sudre CH, May A, Antonelli M, Murray B, Varsavsky T, et al. Changes in symptomatology, reinfection, and transmissibility associated with the SARS-CoV-2 variant B.1.1.7: an ecological study. Lancet Public Health. 2021 Apr 12;6(5):e335–45.
- Davies NG, Jarvis CI, Edmunds WJ, Jewell NP, Diaz-Ordaz K, Keogh RH. Increased mortality in community-tested cases of SARS-CoV-2 lineage B.1.1.7. Nature. 2021 Mar 15;1–5.
- Muik A, Wallisch A-K, Sänger B, Swanson KA, Mühl J, Chen W, et al. Neutralization of SARS-CoV-2 lineage B.1.1.7 pseudovirus by BNT162b2 vaccine–elicited human sera. Science. 2021 Mar 12;371(6534):1152–3.
- Garcia-Beltran WF, Lam EC, St. Denis K, Nitido AD, Garcia ZH, Hauser BM, et al. Multiple SARS-CoV-2 variants escape neutralization by vaccine-induced humoral immunity. Cell. 2021 Apr;184(9):2372-2383.e9.
- Haas EJ, Angulo FJ, McLaughlin JM, Anis E, Singer SR, Khan F, et al. Impact and effectiveness of mRNA BNT162b2 vaccine against SARS-CoV-2 infections and COVID-19 cases, hospitalisations, and deaths following a nationwide vaccination campaign in Israel: an observational study using national surveillance data. The Lancet. 2021 May 15;397(10287):1819–29.
- Abu-Raddad LJ, Chemaitelly H, Butt AA. Effectiveness of the BNT162b2 Covid-19 Vaccine against the B.1.1.7 and B.1.351 Variants. New England Journal of Medicine. 2021 May 5;NEJMc2104974. doi: 10.1056/NEJMc2104974.
- Emary KRW, Golubchik T, Aley PK, Ariani CV, Angus B, Bibi S, et al. Efficacy of ChAdOx1 nCoV-19 (AZD1222) vaccine against SARS-CoV-2 variant of concern 202012/01 (B.1.1.7): an exploratory analysis of a randomised controlled trial. The Lancet. 2021 Apr 10;397(10282):1351–62.
- Madhi SA, Baillie V, Cutland CL, Voysey M, Koen AL, Fairlie L, et al. Efficacy of the ChAdOx1 nCoV-19 Covid-19 Vaccine against the B.1.351 Variant. New England Journal of Medicine. 2021 May;384(20):1885–98.
- Mercado NB, Zahn R, Wegmann F, Loos C, Chandrashekar A, Yu J, et al. Single-shot Ad26 vaccine protects against SARS-CoV-2 in rhesus macaques. Nature. 2020 Oct;586(7830):583–8.
- Shinde V, Bhikha S, Hoosain Z, Archary M, Bhorat Q, Fairlie L, et al. Efficacy of NVX-CoV2373 Covid-19 Vaccine against the B.1.351 Variant. New England Journal of Medicine. 2021 May;384(20):1899–909.
- Faria NR, Mellan TA, Whittaker C, Claro IM, Candido D da S, Mishra S, et al. Genomics and epidemiology of the P.1 SARS-CoV-2 lineage in Manaus, Brazil. Science. 2021 May 21;372(6544):815–21.
- Sabino EC, Buss LF, Carvalho MPS, Prete CA, Crispim MAE, Fraiji NA, et al. Resurgence of COVID-19 in Manaus, Brazil, despite high seroprevalence. The Lancet. 2021 Feb 6;397(10273):452–5.
- Tada T, Zhou H, Dcosta BM, Samanovic MI, Mulligan MJ, Landau NR. The Spike Proteins of SARS-CoV-2 B.1.617 and B.1.618 Variants Identified in India Provide Partial Resistance to Vaccine-elicited and Therapeutic Monoclonal Antibodies. bioRxiv. 2021 May 16;2021.05.14.444076.
- Hoffmann M, Hofmann-Winkler H, Krüger N, Kempf A, Nehlmeier I, Graichen L, et al. SARS-CoV-2 variant B.1.617 is resistant to Bamlanivimab and evades antibodies induced by infection and vaccination. bioRxiv. 2021 May 5;2021.05.04.442663.
- Bernal JL, Andrews N, Gower C, Gallagher E, Simmons R, Thelwall S, et al. Effectiveness of COVID-19 vaccines against the B.1.617.2 variant. medRxiv. 2021 May 24;2021.05.22.21257658.
- COVID-19 vaccine efficacy summary [Internet]. Institute for Health Metrics and Evaluation. 2021 [cited 2021 Jun 6]. Available from: http://www.healthdata.org/covid/covid-19-vaccine-efficacy-summary
- Wu K, Choi A, Koch M, Elbashir S, Ma L, Lee D, et al. Variant SARS-CoV-2 mRNA vaccines confer broad neutralization as primary or booster series in mice. bioRxiv. 2021 Apr 13;2021.04.13.439482.
- Moderna Announces Positive Initial Booster Data Against SARS-CoV-2 Variants of Concern | Moderna, Inc. [Internet]. [cited 2021 Jun 6]. Available from: https://investors.modernatx.com/news-releases/news-release-details/moderna-announces-positive-initial-booster-data-against-sars-cov/