- 新型コロナウイルス感染症(COVID-19)の流行は、政治的状況、医療体制、ワクチン接種状況などで国や地域ごとに大きく異なるが、世界の人々にワクチンが行き渡るまでは終わりが見えない。
- もうしばらく続くであろうパンデミックの中で、いかに感染爆発を防ぎながら安全に社会経済活動を続けていくかが直近の課題である。
- 我々は、診断に用いるPCR検査を唾液検体とプール法による社会的検査に活用し、Ct値を参考に社会活動度を推奨することを提唱している。
- この寄稿では、Ct値と感染性の関連性、鼻咽頭スワブと唾液のPCR検査感度・効率性の比較、プール法の検証などの研究結果を紹介し、世田谷区が独自に取り組んできた社会的検査の結果を紹介する。
- 変異株の出現と流行の背景には、集団免疫が獲得できていないコミュニティで無症状感染者が気づかない間に感染を広げ蔓延させてしまうことが挙げられる。一部の変異株には抗体製剤やワクチン接種による抗体反応を回避するものもあり、新たな変異株の出現や蔓延を防ぐためには、定期的に検査し感染者を見つけ、Ct値に応じて隔離すること、ワクチン接種を進め集団免疫獲得を目指すことが重要である。
- 重要なことは、医療機関で行う医学的検査と、無症状者を対象とする社会的検査の目的の違いを理解することである。
はじめに
2020年3月に世界保健機関(WHO)が新型コロナウイルス感染症(COVID-19)を世界的大流行(パンデミック)と宣言してから、すでに1年が過ぎた。類を見ないスピードのワクチン開発により、裕福な国を中心にワクチン接種が進んでいるが、世界的には日々の新規感染者数、重症患者数、死者数いずれを見てもまだ収束に向かっているとは言えない状況である。
感染拡大防止に重要なことは、なるべく早く感染者を見つけることであり、診断には新型コロナウイルス(SARS-CoV-2)のターゲット遺伝子を増幅させ検出するPCR検査が最も多く用いられている。目的に応じたPCR検査の分類として、診断・治療目的に行う医学的検査(行政検査)と、他者へ感染を拡大する可能性がないことを確認するためにスクリーニングとして行う社会的検査がある。前者はあくまでも患者が治療を受けるために新型コロナウイルスに感染していることを確認するための診断的検査であるが、後者は、検査結果を陽性・陰性だけではなく、特異遺伝子が陽性となるまでのサイクル数である「Ct値」から推測されるウイルス量を勘案して、社会的活動の目安を示すことで、感染拡大防止と社会経済活動の両立を目指すためのものであり、検査の目的が異なる。
この寄稿では、日本におけるこれまでの感染状況について述べ、社会的PCR検査のコンセプトとなるCt値の解釈について説明する。また、社会的スクリーニングで重要になってくる、多検体検査を可能とするプール法について、これまでわかってきた知見について紹介するとともに、世田谷区の取り組みの事例や、近日、非常に大きな問題となっている変異株について概略する。
日本におけるCOVID-19の流行状況
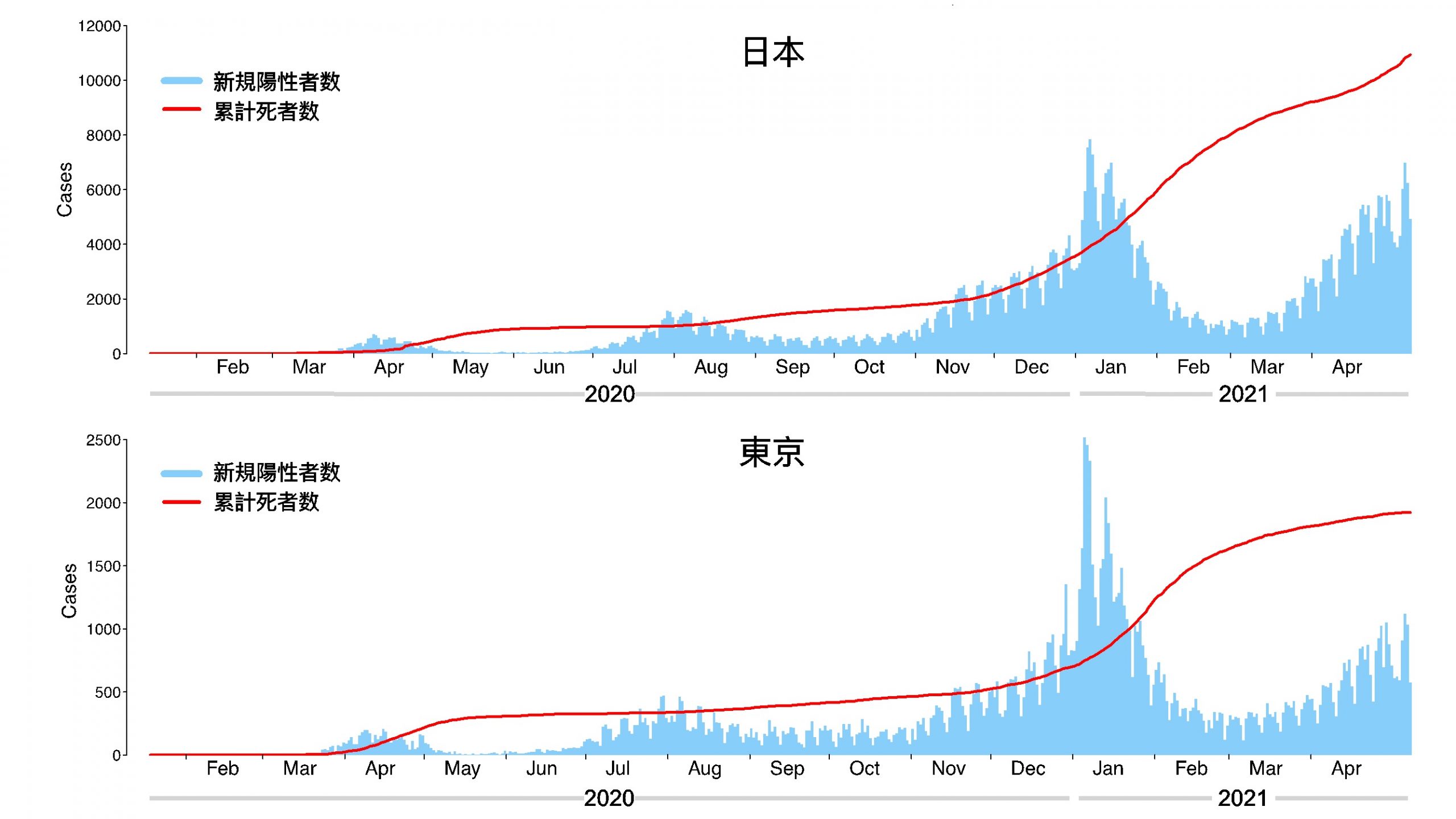
まず、日本および東京における一日あたりの新規感染者数と累積死亡者数を示す【図表1】。この図を見ると、日本、東京共にこれまで4つの流行の波があり、初期の2波より第3波、第4波の方が一日あたりの新規感染者数のピークが高いこと、また、全体としての一日あたりの新規感染者数のピークは1月であったことがわかる。
日本政府はこれまで、2020年4月7日〜5月25日、2021年1月8日〜3月21日、そして2021年4月25日〜6月20日(5月31日時点)と3回緊急事態宣言を発令し、飲食店やイベント施設などの時短営業や休業、テレワーク、県外への移動の自粛などを要請し、マスク着用、手指衛生、3密(密閉、密集、密接)対策などを呼びかけてきた。2020年は、アメリカやヨーロッパ、ブラジルなど他の国々と比べると日本の感染流行状況は比較的少ない方であったが、2021年に入り、各国、特にアメリカやヨーロッパ、イスラエルなどでワクチン接種が進み種々の行動制限が緩和され経済活動が活発化する中、日本はワクチン接種のスピードが極めて遅く、各種変異株が予想を上回る勢いで増え、医療施設への圧迫と社会経済の停滞から脱することが出来るのはまだ先と推察される。
| 図表1 |
| 日本および東京都における新規感染者数と累計死者数の推移 |
| 日本(上パネル)と東京都(下パネル)における新規感染者数と累計死者数。日本のデータは https://www.mhlw.go.jp/stf/covid-19/open-data_english.htmlより;東京都のデータはhttps://stopcovid19.metro.tokyo.lg.jp/en. よりダウンロードし解析(ダウンロード日:2021年5月12日)。 |
 |
PCR検査のCt値とその解釈方法
COVID-19の診断に用いるPCR検査
新型コロナウイルス感染症の診断に最もよく行われている検査が、RT-qPCR法(以下PCR検査)と抗原定性検査である。PCR検査は、採取した検体(唾液、鼻咽頭スワブなど)の中に存在するウイルスの特定のターゲット遺伝子を増幅させ検出する検査法で、結果の評価に用いるCt (Cycle Threshold) 値は、検出可能な閾値に達するまでPCR にて何回増幅を行ったかを示す数値を表す。Ct 値の数値が低ければ低いほどウイルス量が多く、高ければ高いほど少なくなる。日本の行政検査におけるPCR検査はCt=40未満を陽性としている(*注)。
*Ctのカットオフ値は各国、専門家の意見により異なり、Ct値は様々な要因(検査機器・試薬・ターゲット遺伝子、増幅効率等)によって数値が変動することに注意。
唾液 vs. 鼻咽頭スワブ検体
COVID-19の診断用PCR検査のための検体は鼻咽頭スワブが最も多く使用されてきた。鼻咽頭スワブは、鼻腔の奥から検体を採取するため、医療従事者による採取が必要であり、また、感染予防のために個人用防護具(PPE)の使用が必要で、人的・物的コストがかかる。また、採取時に咳やくしゃみが出やすく、飛沫感染のリスクがある。
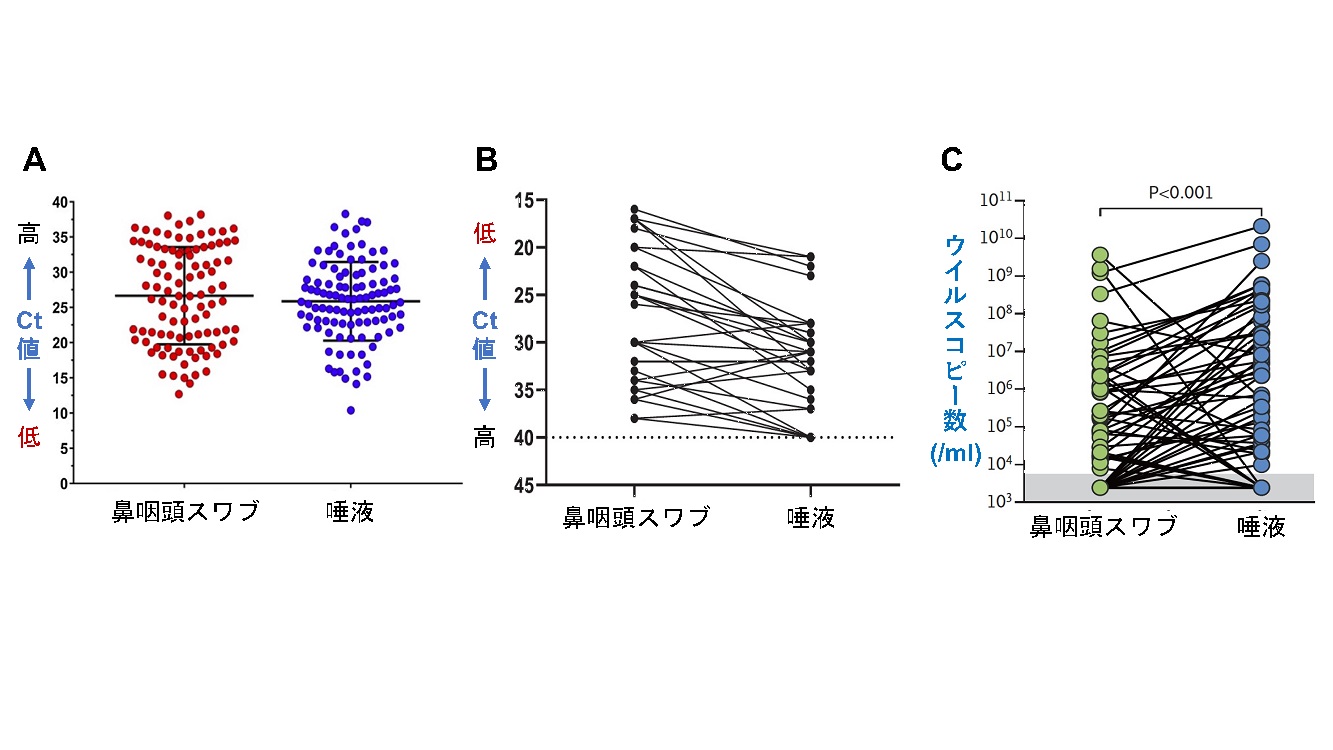
一方、唾液の採取は非侵襲的かつ自己採取が可能で、医療従事者への負担や感染リスク、検査を受ける人の苦痛が減り、PPEなどの物的コストも節約できる。そのため、特に無症状の人を対象に行うスクリーニングなど一度に多くの検体を採取する際に特に有用である。鼻咽頭スワブと唾液のペア検体を用いてPCR検査の結果を比較検証した研究は多く発表されており、検体間でCt値や検体中のウイルス濃度に有意な差がないとする報告[1]【図表2A】、鼻咽頭スワブの方が多い(Ct値が低い)とする報告[2]【図表2B】、唾液中の方が多い(Ct値が低い)とする報告[3]【図表2C】、など様々である[4, 5]。
鼻咽頭スワブと唾液の核酸増幅検査(PCR法を含む)の比較検証を行った複数の論文を系統的レビューとメタアナリシスを行った研究では、鼻咽頭スワブ検体による検査の感度・特異度も決して完璧ではないことを考慮し解析を行った結果、唾液検体の感度は83.2%、特異度は99.2%で、鼻咽頭スワブ検体は感度が84.8%、特異度が98.9%で、唾液検体を用いた核酸増幅検査の診断の正確性は鼻咽頭スワブ検体の場合と同等であるという結論であった[6]。
| 図表2 |
| 鼻咽頭スワブと唾液の検体間のPCR検査Ct値・ウイルス量の比較 |
| 鼻咽頭スワブと唾液のペア検体でSARS-CoV-2のPCR検査のCt値及びウイルスRNAコピー数を比較した研究の代表例を示す。 A. Herreraらは鼻咽頭スワブ・唾液間でN1, N2のどちらのターゲット遺伝子においてもCt値に統計学的に有意な差は見られかったことを示した(図はN1)。 B. Baratらは29のペア検体の比較では、N1, N2のどちらのターゲット遺伝子においても鼻咽頭スワブ検体の方が唾液よりCt値が低い傾向にあることを示した(図はN1, Wilcoxonの符号順位検定にてp<0.001)。 C. Wyllieらは、70名のCOVID-19患者のペア検体を比較し、PCR検査のN1のCt値より求めたSARS-CoV-2のRNAコピー数が、唾液の方が鼻咽頭スワブよりも有意に多いことを示した(Wilcoxonの符号順位検定にてp<0.001)。 |
 |
| AはHerrera LA et al., Int J Infect Dis 2021; BはBarat B et al., J Clin Microbiol 2020; CはWyllie AL et al., N Engl J Med 2020の図より改変 |
Ct値とウイルス量・感染性との関係
PCR検査は、極めて微量のウイルス遺伝子断片を検出することが出来ることから、カットオフ値が40の検査で「陽性」と判定されても、実際には他者への感染リスクがほとんどない可能性もあることが指摘されている。これまでPCR検査のCt値と感染性の関係性において、いくつかの知見が得られている。
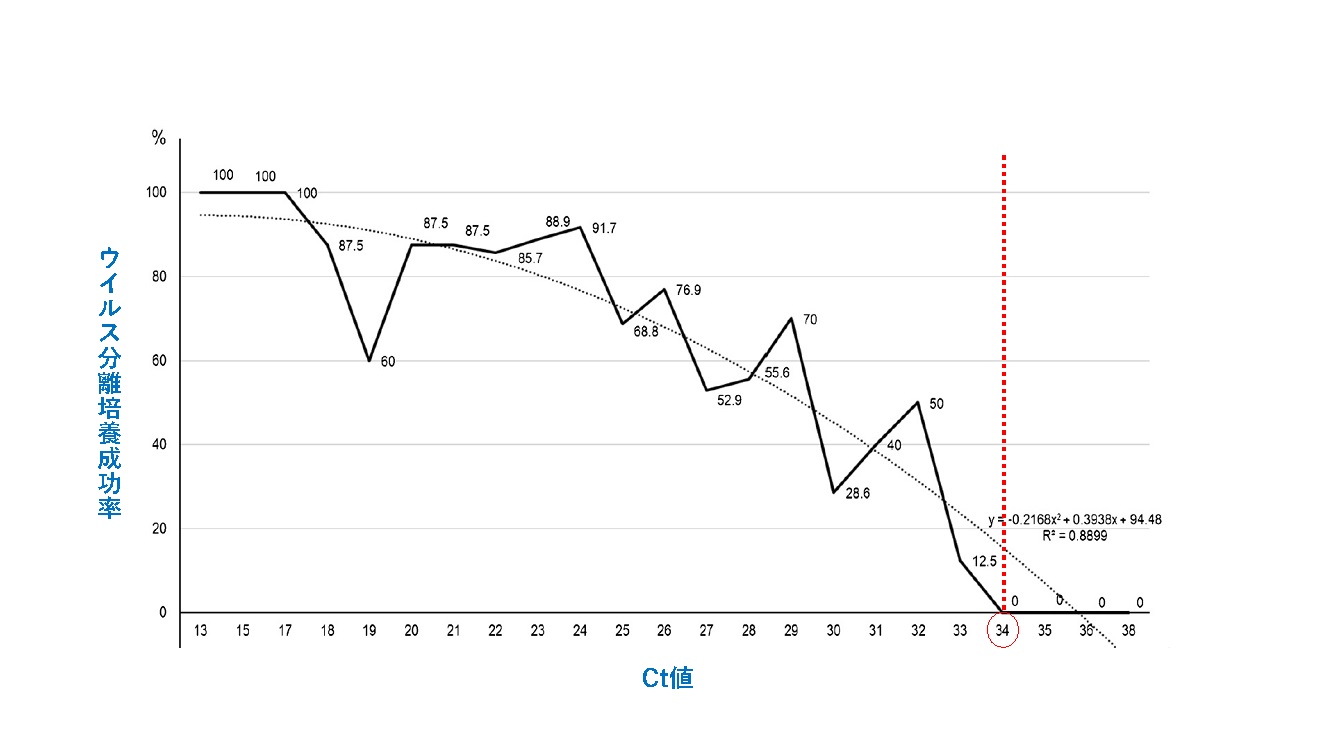
1: フランスの研究グループは、COVID-19患者の鼻咽頭スワブ検体を用いて培養細胞に感染実験を行い、患者検体のPCR検査Ct値が上がるほど、また症状発現後日数が経てば経つほど、ウイルス分離培養成功率が下がること、そして具体的にはCt値が34を超えると培養細胞への感染が成立しないことを示した[7]【図表3】。
2: カナダの研究グループは、COVID-19患者の鼻咽頭スワブ・気管内分泌物検体を用いて培養細胞に感染実験を行い、患者検体のPCR検査Ct値が24を超えると、また症状発現後8日以降に採取した検体では、培養細胞への感染性がないことを示した[8]【図表4】。
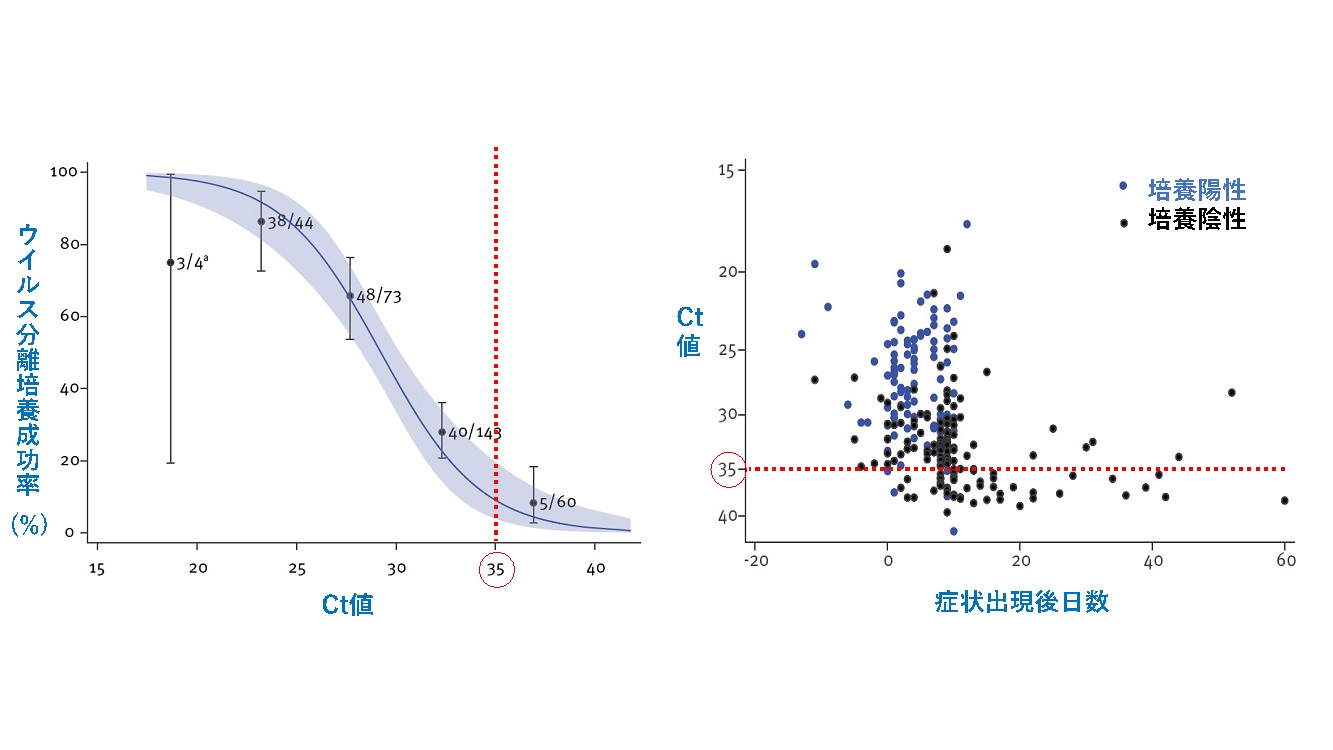
3. イギリスの研究グループは、COVID-19患者の上気道検体を用いて培養細胞に感染実験を行い、患者検体のPCR検査Ct値が上がるにつれウイルス分離培養成功率が下がり、Ct値が35を超えると成功率は8%にまで減少することを示した[9]【図表5左】。また、Ct値は無症状、軽度〜中等症、重症のグループ間で有意な差は見られなかった。症状のあった患者の検証では、ウイルス分離培養成功率は症状発症時前後がピークで、発症後10日では6%にまで低下していた[9]【図表5右】。
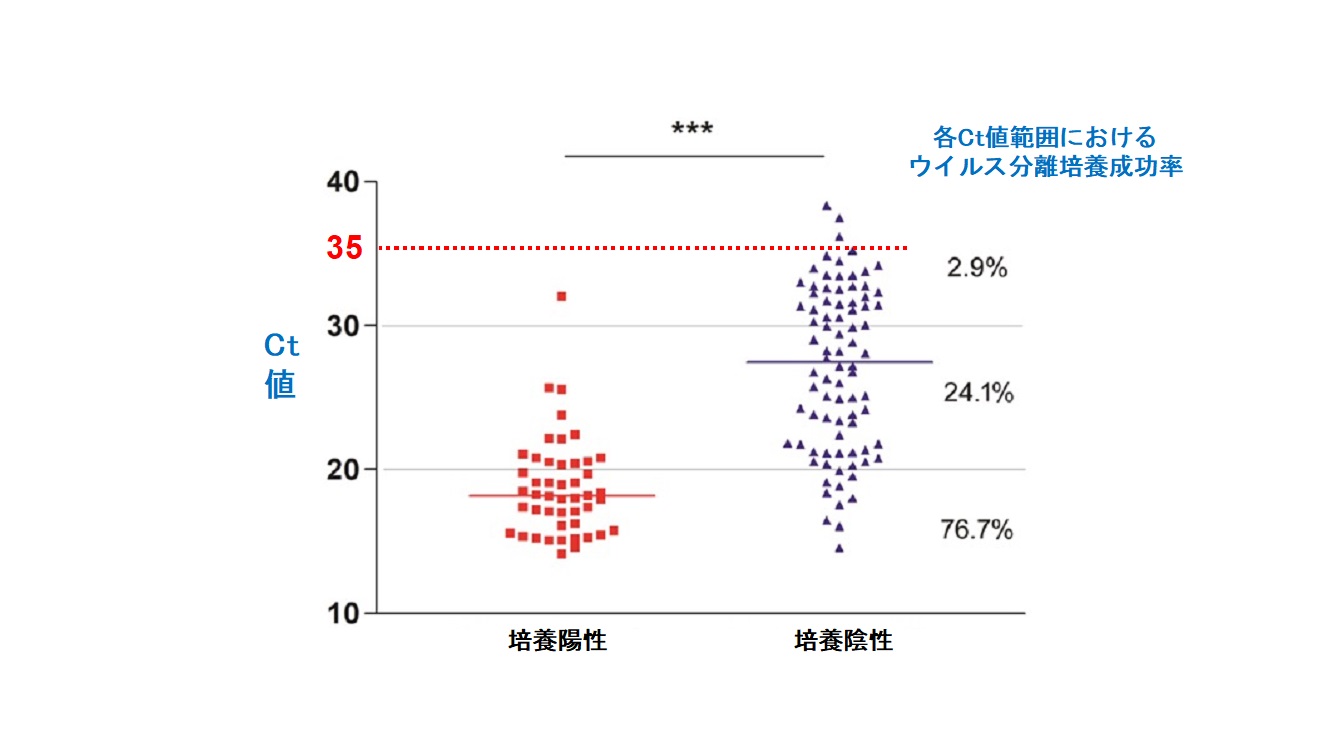
4. アメリカの研究グループは、COVID-19患者の鼻咽頭スワブ検体を用いて培養細胞に感染実験を行い、ウイルス分離培養陽性群は陰性群と比べて検体のPCR検査Ct値が統計学的に有意に低いこと、また、ウイルス分離培養成功率は患者検体のPCR検査Ct値が10-20の場合76.7%、Ct値20-30の場合24.1%、Ct値30-40の場合2.9%であることを示した[10]【図表6】。
5. 本邦からは河岡らのグループが、COVID-19患者の各種検体(うがい液、唾液、鼻咽頭スワブ、喀痰など)のPCR検査のCt値と各種迅速抗原検査の感度を比較検証した研究において、PCR検査Ct値が30を上回ると、ウイルスの分離培養は得られないことを示した[11]。
以上、上に挙げた報告における培養細胞モデルにおける感染成立のCt値のカットオフには少しばらつきがあるものの、共通して言えることは、Ct値が35を超えるとSARS-CoV-2のウイルス複製能はもはや皆無に近いと考えられることだ。
| 図表3 |
| RT-PCRのCt値と培養細胞における感染性との関係 |
| 診断確定後の155名のCOVID-19患者の鼻咽頭スワブ検体を用いてP C R検査のCt値(ターゲット遺伝子:E遺伝子)とVero細胞への感染成立との関連について検証。ウイルス分離培養成功率は、Ct値が上がるにつれ下がり、Ct値が34では0%になった。 |
 |
| La Scala B et al., Eur J Clin Microbiol Infect Dis 2020の図より改変 |
| 図表4 |
| RT-PCRのCt値及び発症後日数と培養細胞における感染性との関係 |
| 診断確定後の90名のCOVID-19患者の鼻咽頭スワブ及び気管内分泌物検体を用いてP C R検査のCt値(ターゲット遺伝子:E遺伝子)とVero細胞への感染成立との関連について検証。ウイルス分離培養陽性群は、陰性群と比べて統計学的に有意な差を持ってPCR検査のCt値が低く、発症後の日数が少ないという結果を示した。 |
 |
| Bullard J et al., Clin Infect Dis 2020 の図より改変 |
| 図表5 |
| RT-PCRのCt値、発症後日数、細胞実験におけるウイルス分離培養成功率との関係 |
| 診断確定後のCOVID-19患者の上気道(鼻、喉、鼻咽頭)検体を用いてP C R検査のCt値(ターゲット遺伝子:RdRp遺伝子)とVero細胞への感染成立との関連について検証(左図:n=324)。ウイルス分離培養成功率は、Ct値が上がるにつれ下がり、Ct値が35を超えると8%にまで減少した。また、症状のあった患者の症状出現後日数とP C R検査のCt値、分離培養陽性との関連性について検証(右図:n=246)した結果、ウイルス分離培養成功率は症状出現時がピークで、第一週目は74%、第二週目は20%、症状出現後10日経過すると6%にまで減少した。 |
 |
| Singanayagam A et al., Euro Surveill 2020の図より改変 |
| 図表6 |
| ウイルス分離培養陽性群と陰性群の患者検体PCRのCt値の分布 |
| 診断確定後の131名のCOVID-19患者の鼻咽頭スワブ検体を用いてVero細胞への感染が成立した群としなかった群に分け、患者検体の PCR検査のCt値(ターゲット遺伝子:検査系によってSまたはNsp2遺伝子) の分布を表示。ウイルス分離培養陽性群はPCR検査のCt値の平均が18.8(標準偏差3.4)、中央値18.17で、陰性群(平均27.1、標準偏差5.7、中央値27.5)と比べて有意に低かった(***p値<0.0001)。ウイルス分離培養成功率はCt値が10-20の範囲で最も高く76.7%で、Ct値20-30で24.1%、Ct値30-40では2.9%に下がった。 |
 |
| Victoria Gniazdowski V et al., Clinical Infectious Diseases 2020より改変 |
感染拡大防止と社会経済活動を両立させるためのCt値を参考にした推奨社会活動度
感染拡大の一つの原因として、無症状のまま、あるいは症状が出現する前に、知らないうちに感染を広げてしまうことがある。全ての社会経済活動を閉ざすと確かに感染拡大は防げるかもしれないが、その地域・国の経済や生活に大きなダメージを与えてしまう。上に挙げた研究報告から、PCR検査で陽性という結果が出ても、Ct値が高い場合は、他者への感染のリスクが極めて低く、社会活動を制限する必要はないと思われる。
私たちは、最近発表した論文において、Ct値を一つの目安として、社会活動範囲の目安を提唱した[12]【図表7】。
- Ct値が30未満の場合、他者への感染リスクが極めて高いと考え、速やかに隔離及び接触者追跡を開始する。検査を受けた人には医療機関を受診し、必要な治療を受けるよう指導する。
- Ct値が30-34の場合、他者への感染リスクは中等度あると考え、人の集まる場所にはいかず、自主的に隔離をすることを推奨。
- Ct値が34-37の場合、他者への感染リスクは低いと考えられるが、感染早期の可能性もあるため、再検査を促し症状出現がないか気をつけてモニターしつつ、社会活動の維持を可とする。
- Ct値が37より大きい場合、他者への感染リスクはないと考え、通常通りの社会活動を継続可能とする。しかし、一度のPCR検査の結果に頼るのではなく、定期的な検査を推奨し、症状や接触歴などを含め総合的に判断することが重要である。
| 図表7 |
| 推奨する社会的検査におけるPCR検査のCt値による社会的活動の目安 |
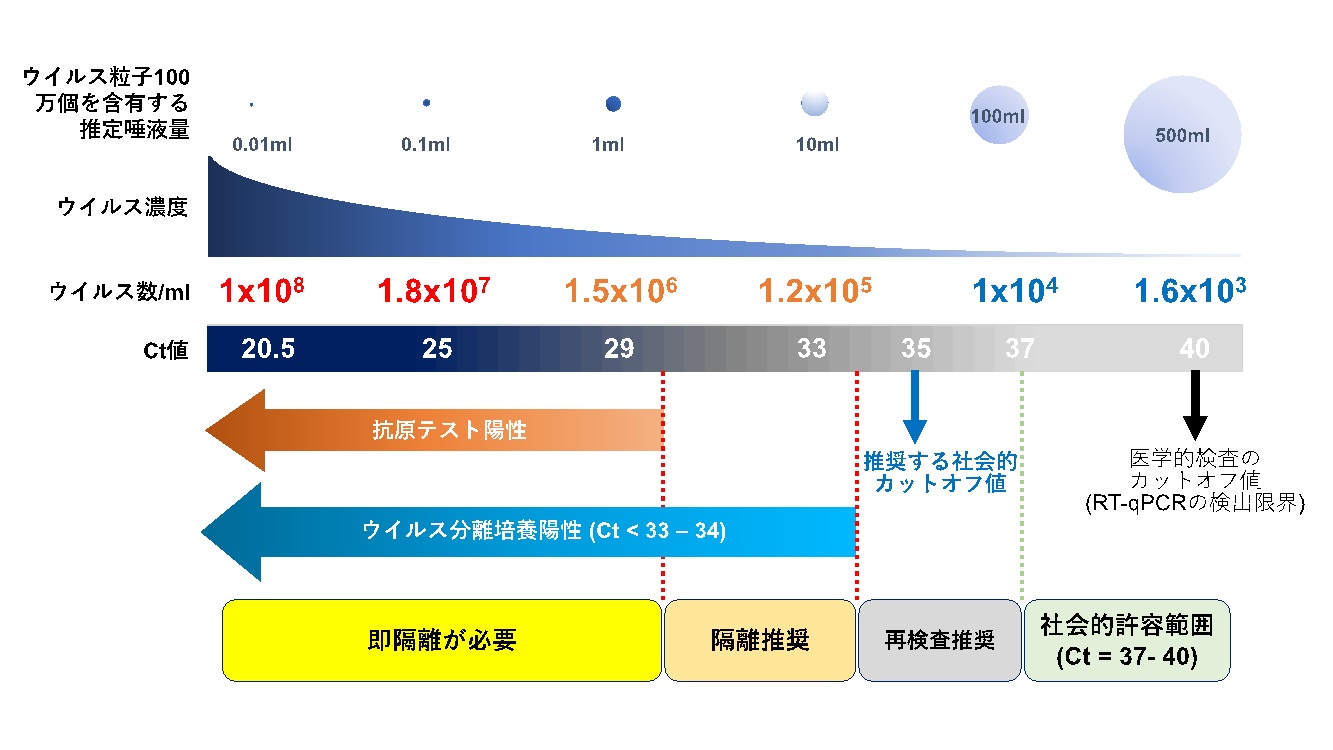
| 筆者らが提唱している社会的PCR検査のCt値による社会経済活動の指標の目安[12]。社会的なスクリーニング検査においては、自己採取が可能で安価に出来る唾液検体を用いることを念頭に、ウイルス粒子100万個を含有する推定唾液量を図の上に示している。各Ct値におけるウイルス粒子100万個を含有する推定唾液量、ウイルスコピー数/mlは、米国のイェール大学の研究者を中心に発表された論文[3]の数式を用いて推測。ウイルス分離培養陽性のCt値は、過去の論文報告[7-11]を元に、厳しめのカットオフ値を示している。従来の医学的検査のカットオフ値が検出限界として一般的にCt値40であるのに対し、新たに提唱する社会的検査のカットオフ値は、Ct値と培養細胞におけるウイルス分離培養成功率との関連性の研究報告[7-11]をもとに設けており、これにより被検者の再検査を促しつつも社会活動を継続できるようにし、感染拡大防止と社会経済活動の両立を目指すものである。 |
 |
| Oba J et al., Keio J Med 2021より改変 |
プール法の意義
行政検査・医学的検査で行われる診断のためのPCR検査は、個々の検体を別々に検査する個別検査が行われているが、無症状の人を対象とした大規模な社会的スクリーニング検査を行う場合、コストや効率性から複数の検体をまとめて一つの検体としてPCR検査を行うプール法の有用性が世界各国から報告されている。
プール法では、一つのプールにまとめて測定したPCR検査の結果が陰性であれば、そこに含まれていた全ての検体が陰性であるとみなされ、陽性であれば検体を個別に再検査し、どの検体が陽性であるかを判定する[13]。鼻咽頭スワブ検体、唾液検体どちらにおいても、又、採取した検体を直接PCR反応する場合でも、検体からRNAを抽出した後にPCR反応を行う場合でも、COVID-19のプール式PCR検査の有用性が報告されている[13, 14]。
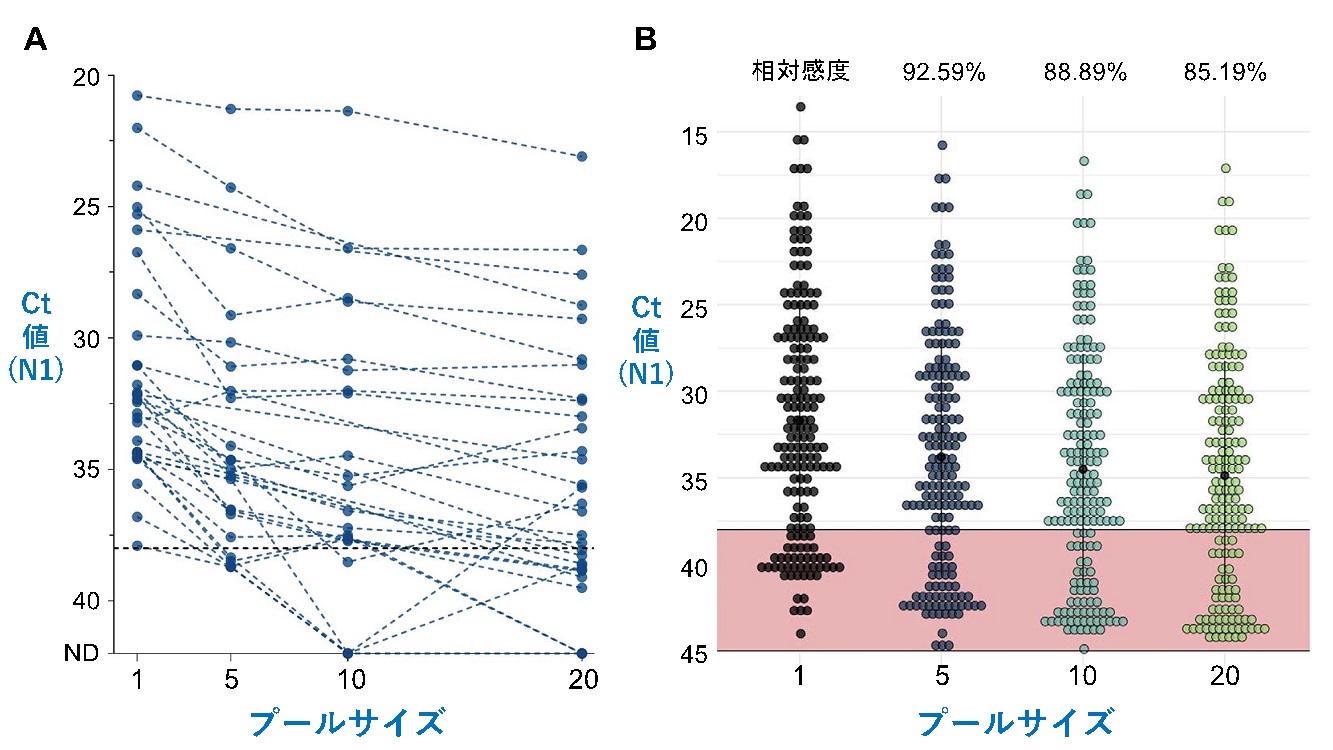
プール法において懸念されるのは、検体が希釈されることにより本来陽性となる検体を見逃してしまう可能性、つまり感度の低下である。Watkinsらは、陽性と判明した唾液検体を陰性と判明した検体と異なる比率 (1:4, 1:9, 1:19)でプールを作成しPCR検査を行い評価し、個別検査と比べた時にCt値が5倍希釈では2.2、10倍希釈では3.1、20倍希釈では3.6上昇し、感度は5倍希釈では7.4%、10倍希釈では11.1%、20倍希釈では14.8%低下することを示した[14]【図表8A, 8B】。しかし、実際に個別検査で「陽性」の検体がプール法で「偽陰性」になるのは、元々のCt値が35前後と高い検体であることが多く、他者への感染リスクが高い人を見つける目的の社会的検査においては、より多くの検体を検査できるプール法がより適していると言える。プール法のサイズを検討する時に考慮に入れるべき要素は、その地域の有病率又は検査陽性率である。有病率・検査陽性率が極めて低い地域では、プールサイズを大きくする(10-30)と効率性と節約効果が高いが、有病率が高くなるにつれてプールサイズを小さくする方が効率性に優れ、あまりにも流行している際にはプール法の利点は消失することが指摘されている[14-16]【図表9】。
| 図表8 |
| プール法によるPCR検査のCt値、感度への影響 |
| A. プールサイズ(一つのプールに入れる検体の数)が大きくなればなるほど、PCR検査Ct値も上昇する。個別検査(プールサイズ1)で陽性と判定された検体が5倍、10倍、20倍と希釈された際のCt値の変化が点線で繋がれて示されている。 B. プールサイズが大きくなるにつれ、陰性と判定される検体が増える。WatkinsらはPCR検査のカットオフ値を38と設定しており、実線以下ピンク色で色付けされている部分は陰性と判定されている。個別検査と比較した時の相対感度は、プール数5で92.59%、プール数10で88.89%、プール数20で85.19%と計算された。 |
 |
| Watkins AE et al., Emerg Infect Dis 2021より改変 |
| 図表9 |
| 有病率・検査陽性率と効率的なプールサイズの関係 |
| A. Regenらは、至適プールサイズ=1.24 x 検査陽性率-0:466の数式を用いてそれぞれの検査陽性率(論文中ではtarget prevalence=positive/total samplesと表記)における最も効果的なプールサイズを示し、検査陽性率が低い時(<0.02, 2%未満)にはプールサイズを上げ効率性を高めることができることを示唆した。 B. Watkinsらは図表8で示した各プールサイズの感度の結果に基づき、1万人の検査をすると仮定した時の、有病率、プールサイズごとに最終的に必要な検査数(プールで陽性となった後の個別検査数も含む)をシミュレーションしグラフ化した。グラフ内に挿入された図は有病率が5%未満の場合の拡大図。Y軸10,000に平行な線は、個別検査(プールサイズ1)の場合の検査数を示している。有病率が0.6%未満(0.006未満)の時はプール数20(緑色の線)が最も効率的でコスト節約効果に優れているが、有病率が2.6%(0.026)を超えると、プール数5(青色の線)がプール数10(水色の線)やプール数20よりも最終的に必要検査数が少なく済むことを示し、さらに有病率が28.1% (0.281)を超えるとプール法ではなく個別検査を行う方が効率的であると推定した。 C. Bishらは、様々な有病率における至適プールサイズを推定する数式モデルを開発した(特異度は100%と想定し、感度は71%, 98%の2パターンでシミュレーション)。図は感度98%での各有病率(1%, 2.5%, 5%, 10%, 15%, 20%, 25%)、プールサイズにおける一人当たりに必要な検査数の推定値を表す。pは有病率(実際のデータ解析では検査陽性率を使用)。またBishらは、有病率が29.2%を超えるとプール法による効率性は消失すると推定した。 |
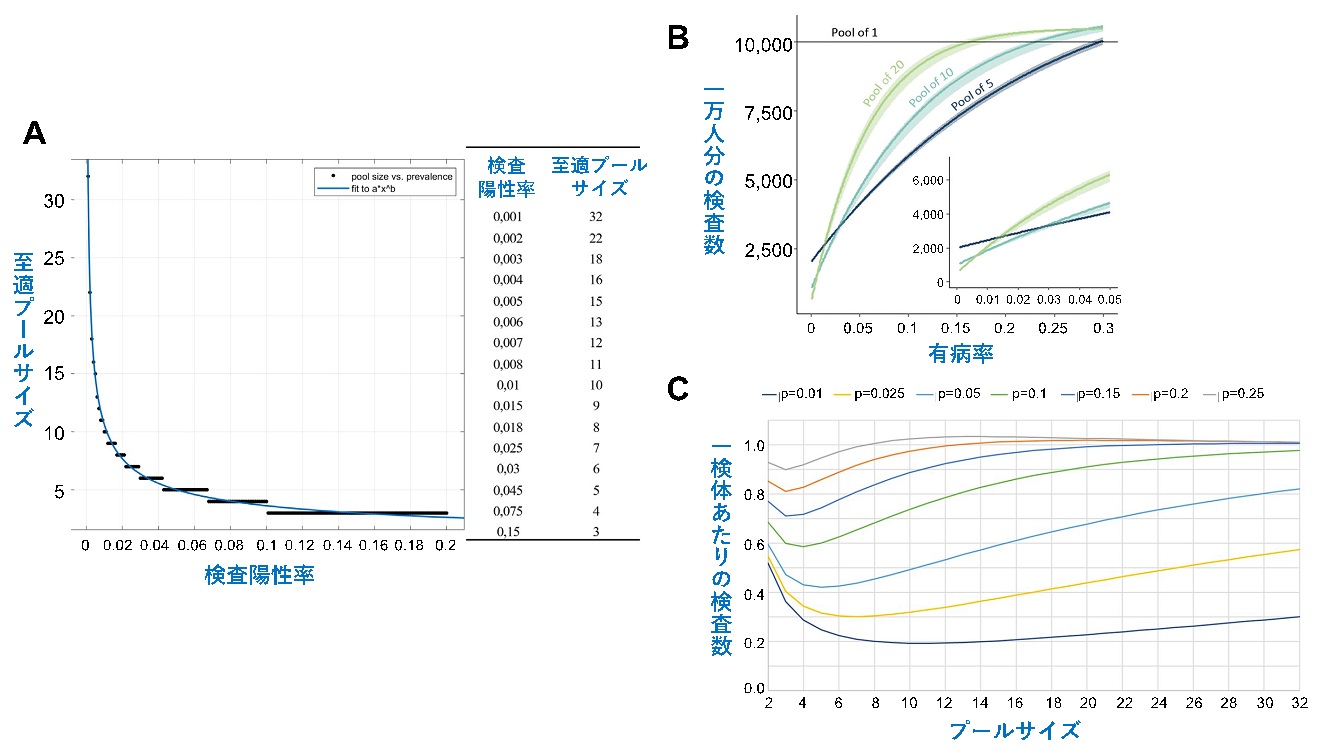 |
| AはRegen F et al., Int J Infect Dis 2020; BはWatkins AE et al., Emerg Infect Dis 2021; CはBish DR et al., PLoS One 2021の図より改変 |
医療現場におけるPCR検査と社会的スクリーニングの目的の違い
有病率が高くなる医療機関でPCR検査を実施する目的は、目の前にいる患者がCOVID-19に罹患していることを確認し、症状に応じて必要な治療を施すためである。陽性の場合、症状の有無や重症度は、Ct値と相関しないことが分かっており、治療方針の決定は全身状態や胸部CTなどの評価に基づく。実際、重症または重篤なCOVID-19患者においては、上気道検体を用いたPCR検査とVero細胞へのウイルス分離培養実験において、症状の持続や悪化、あるいはPCR検査の陽性・陰性の結果に関わらず、感染性ウイルスは発症後0〜20⽇(中央値8⽇)で検出されるが、15⽇後には検出率は5%未満であった [17]。すなわちPCR検査によるウイルス量は病勢を反映しないため、入院重症患者を対象とする鼻咽頭・唾液PCR検査の意義は単にウイルスの存在を証明するに留まり、臨床的有用性は低い。ただし、血清中のウイルスRNA量は、重症度 (ICU入室、侵襲的人工換気)との相関性が指摘されている[18]。
一方、社会的検査の目的は、無症状の人を対象に、気づかない間に感染している人を見つけ、他者への感染性の有無を評価し、感染拡大を防止することである。我々は、社会的検査にて陽性の場合、PCR検査のCt値からウイルス量を推定し、他者への感染リスクを層別化することを提案している【図表7】。例えば、Ct=40の場合には、その人の唾液中のウイルス濃度は低く、ペットボトル1本(500ml)でウイルス100万個の量に相応するが、Ct=25の場合には、わずか0.1ml(水1滴程度)の唾液に100万個のウイルスが含まれることを意味する。同じ「PCR陽性」でも、これだけ放出しているウイルス量が異なっていることに留意して、接触者対応を行うべきである。
疫学的観点から重要となるのは、25〜50%の症例は無症状かごくわずかな症状しかないことである[19]。さらに、無症候性、症候性の感染者より排出されるウイルス量はほぼ同じであり、PCR陽性者のうち、無症候性の10%、症候性の14%の感染者 (Ct≦23.7)が、感染性ウイルスの99%を循環させている[20]【図表10】。こうした事実は、感染対策は症状の有無やPCR陽性/陰性で判断するのではなく、Ct値、すなわち放出されるウイルス量に応じて行うべきであることを示唆している。
社会的スクリーニングでは安価に大量に検査できるプール式検査、自己採取が容易な唾液検体を用いることが現実的に妥当な方法であり、定期的な検査を行うことで他者への感染リスクが高い人を見逃さないことが鍵となる。実際、感度が100%に近い検査を少ない頻度で行うよりも、感度が少し劣っても簡便で迅速、そして安価な検査を頻繁に行う方が他者への感染リスクのある無症状感染者を見つける確率は高いことが指摘されている[21, 22]【図表11】。
| 図表10 |
| 無症候性と症候性の集団におけるウイルス量とスーパースプレッダー |
| ウイルス量を唾液により評価したところ、ウイルス量の分布は無症候性と症候性の集団で類似していた(上図)。無症候性、症候性の陽性者の双方で、僅か2%の感染者が感染性ウイルス粒子の90%を保有していた。コミュニティ間を循環するウイルス粒子の99%は、無症候性陽性者の10%(下図)、症候性陽性者の14%により排出される。 |
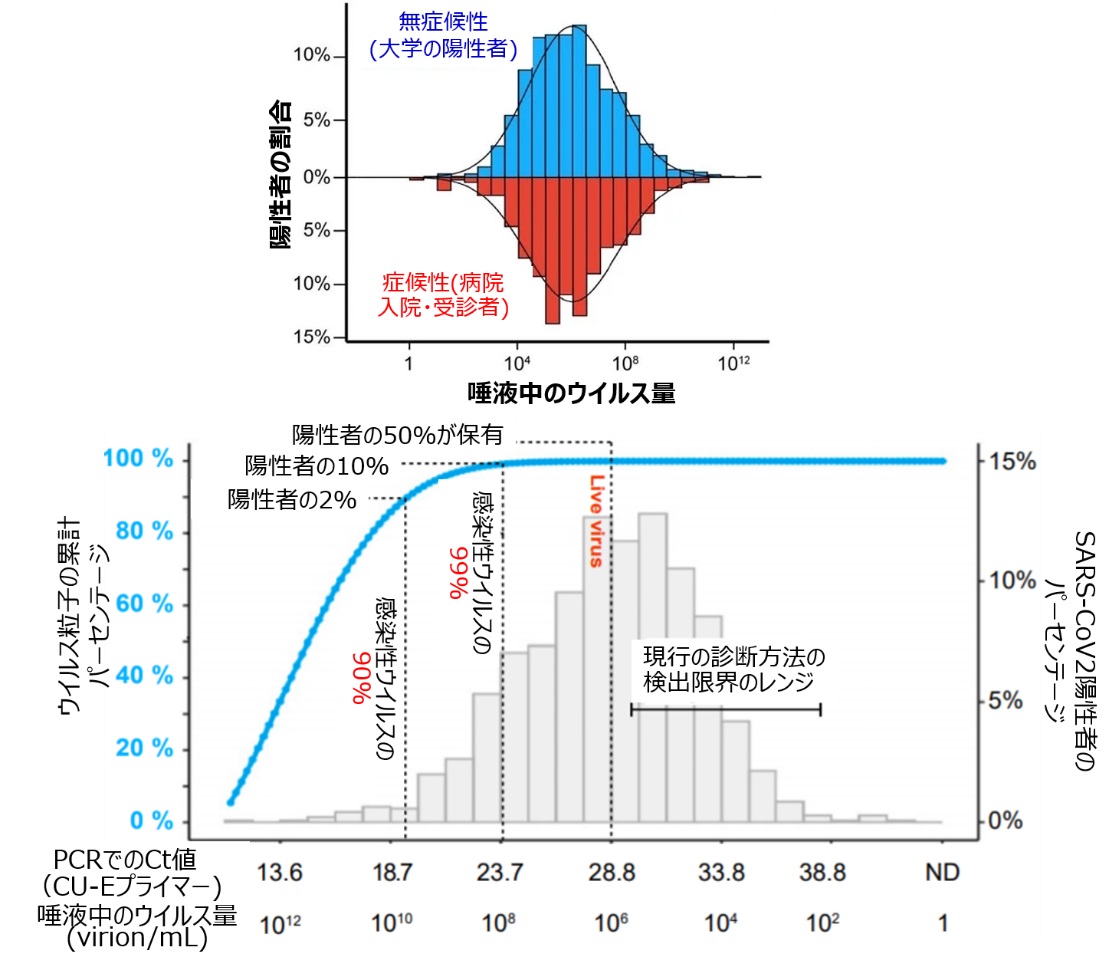 |
| Q Yang, et al., Proc Natl Acad Sci U S A. 2021の図より改変 |
| 図表11 |
| 社会的検査において重要なことは定期的に検査を行うこと |
| 横軸は時間の経過を、SARS-CoV-2感染時の体内のウイルス量の変化が青線で示されている。感染感度に優れた検査はウイルスの存在を検出できるかもしれないが、頻繁に検査しない場合、感染性の既に消失した回復期の感染者を見つけるだけになる場合がある。感度がやや劣るが簡便・迅速・安価なプール法や抗原検査などの検査を頻回に行えば、ウイルス量がピークに達する前後の他者への感染リスクが高い人を見つけられる確率はより高い。 |
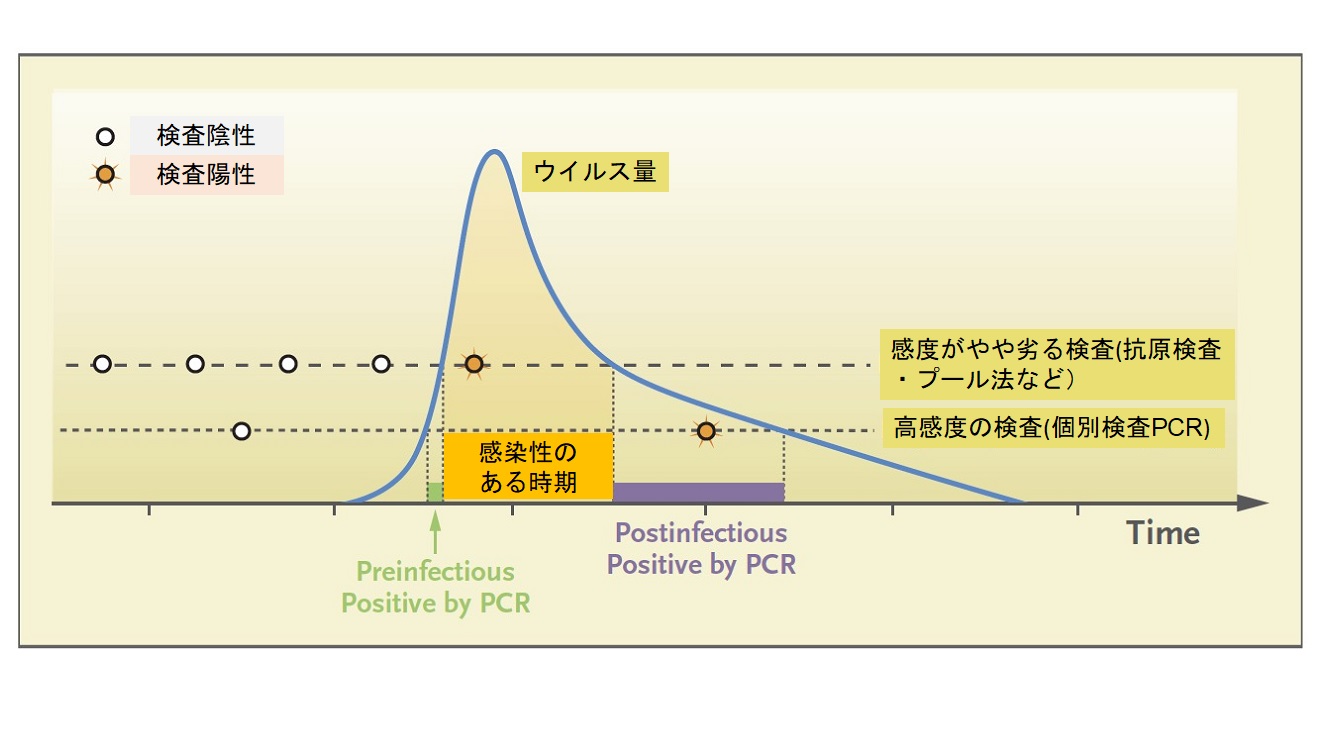 |
| Mina MJ et al., N Engl J Med 2020より改変 |
世田谷区の取り組み
東京都世田谷区では、クラスターを未然に防ぐことを目的として、介護・福祉関係施設の利用者や職員の無症状者を対象として、2020年秋から社会的検査を行なっている。そこで得られた知見は以下の通りである(令和3年3月26日、4月28日、5月28日の世田谷区長記者会見資料参照)。
- 2020年11月〜2021年3月に検査した約12000人の施設利用者・職員のうち約80人がPCR検査陽性であった(全体陽性率:0.65%)。
- 陽性者のうち半数以上においてCt値が30未満と他者への感染リスクが高い結果を示した。
- 陽性者のCt値は年齢や性別と統計学的に有意な関連性を認めなかった。無症状であってもウイルスに感染し、Ct値が低い(ウイルス量が多い)人が年齢・性別に関係なく存在する。
- 定期的なPCR 検査を行っている施設は、そうでない施設と比べてPCR検査陽性者発生率は2分の1に、クラスター発生率は3分の1に抑えられていた。
- クラスター発生施設の約8 割にCt 値20 未満の陽性者が確認された。すなわち、陽性者のCt 値が特に低い場合にクラスターが発生しやすい状況になっていると考えられた。
これらの結果をもとに、世田谷区は今後、社会的検査をより受けやすい仕組みへの見直しを行い、Ct 値が低い陽性者が発生した場合の対応強化(濃厚接触者だけでなく、当該施設もしくはフロア等にいる全ての職員・利用者を対象とした検査を強く促す、追加検査を一週間間隔で複数回実施するなど)に努める方針としている。
変異株について
SARS-CoV-2は、約30kb(29,903塩基)の一本鎖RNAウイルスで、他のウイルスと同様に遺伝子の突然変異を起こす。ある特定の変異を持つウイルスの感染が人々の間で広がり定着すると、元々の変異がなかった野生型ウイルスと区別し変異株と呼ぶ。2020年冬から、世界各国でより感染性の強い注意を喚起する変異株が出現し始めた。代表的な変異株にアルファ株(英国株、B.1.1.7)、ベータ株(南アフリカ株、B.1.351)、ガンマ株(ブラジル株、P.1)があるが、他にも様々な変異ウイルスの報告がされている。英国株、南アフリカ株、ブラジル株はいずれも従来の野生型と比べて感染性が高くなっていることが報告されている[23-25]。これらの変異株には、表面突起のSタンパク質をコードする遺伝子に変異が入っており、これらはいずれも感染・伝播性に影響があるとされるN501Y変異を有する。そのことでヒトの細胞表面の受容体(ACE2受容体)に結合しやすくなっていると考えられている。
英国株と言われるVOC-202012/01株は従来株と比較して実効再生産数が43-90%高く[23, 26]、従来株より感染性が25-40%増加する。その結果、英国内で急速に増加し世界的な感染拡大を生じた。また死亡リスクを55~64%上昇させる[27]。本変異株症例の疫学的特性は、従来株に比べて小児の感染リスクが高い可能性が指摘されている [28]。
感染やワクチン接種により体内で産生される抗体や治療に用いられる抗体製剤は、ウイルスのSタンパク質に結合し細胞への侵入を防ぐが、Hoffmanらは南アフリカ株やブラジル株ではそれらの効果が減弱していることを示し警鐘を鳴らしている[29]【図表12】。これらの株は、中和抗体からの逃避回避とされるE484K変異を有していることが特徴である。
英国株、南アフリカ株、ブラジル株の3つに続いて最近(2021年5月10日)、WHOによりデルタ株(インド株、B.1.617.2)も「世界的に懸念される変異株」として指定された。インド株についてはまだ不明な部分も多いが、感染性が高いことと、免疫回避型の変異も持ち合わせていることが指摘されている[30-32]。幸いなことに、このインド株に対しファイザー製ワクチンとアストラゼネカ製ワクチンの2回接種がイギリス株と同程度に有効であるという報告が出た[33]。
COVID-19の世界的な流行が収束に向かうためには、集団免疫をつけるためのワクチン接種を加速させること、社会的スクリーニングによりコミュニティ内の流行を抑え新たな変異株の発生をなるべく抑え込むこと、が極めて重要だと言える。
| 図表12 |
| 代表的な変異株と抗体免疫、抗体製剤の効果 |
| 左から英国株(B.1.1.7)、南アフリカ株(B.1.351)ブラジル株(P1)のSタンパク質をコードする遺伝子のどこに変異が入っているかを図示している。RBD, 受容体結合ドメイン。TD, 膜貫通ドメイン。下のパネルにはSタンパク質の三量体構造正面像が示されている。S1タンパク質は水色、S1タンパク質内のRBD領域は濃い青〜青紫色、変異したアミノ酸残基は赤色で示されている。 |
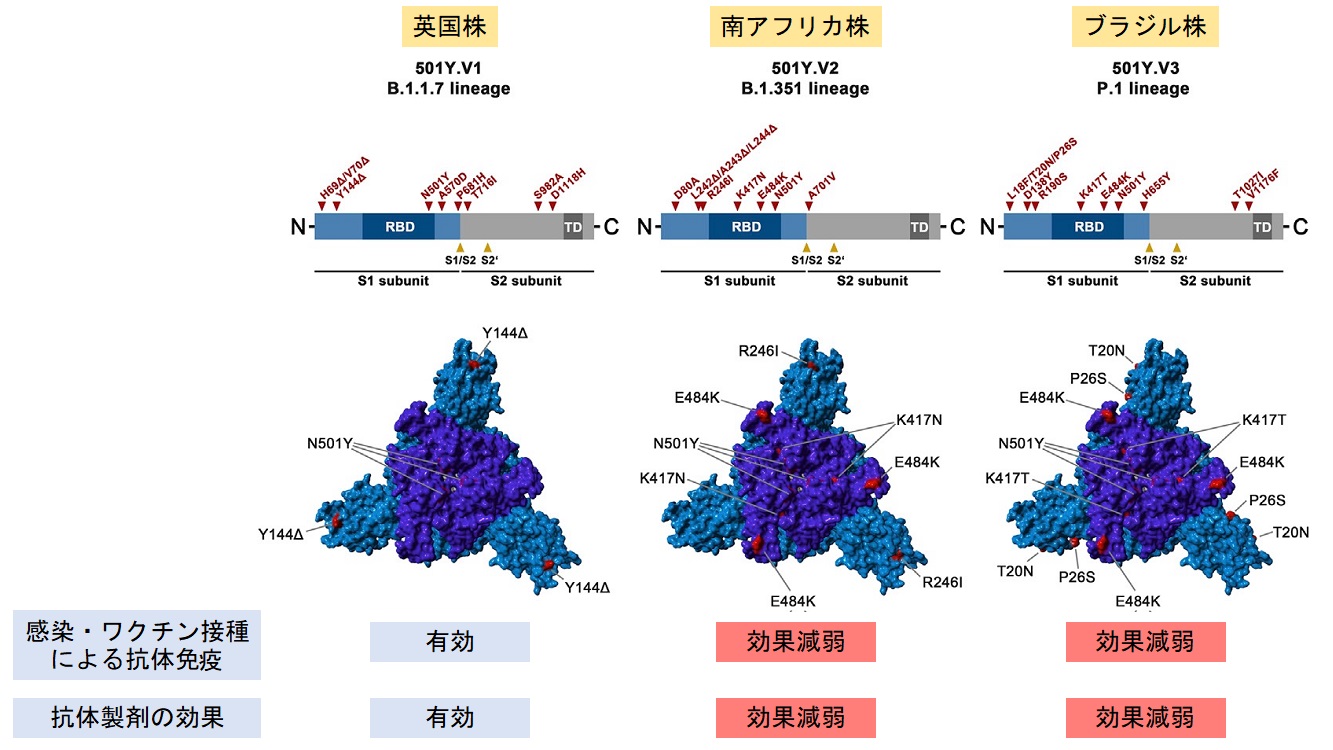 |
| Hoffmann M et al., Cell 2021より改変 |
おわりに
我が国においては、PCR検査体制の遅れが当初から指摘されている。これは、発症者、特に重症者に対する医療対応を優先する中で、PCR検査の目的が新型コロナウイルスに感染していることを証明することに力点が置かれていたため、有症状者に対する限定的かつ確実な検査体制を目指したことに起因する。一方で、中国や欧米諸国では当初から、感染制御の目的でいつでもどこでもPCR検査が受けられる体制を構築し、いわゆるスクリーニング検査体制を強化してきた。
ただ、我が国では緊急事態宣言が発令されているとは言え、欧米に比べれば人口比での感染者数は少なく、幅広いスクリーニング検査を行わなくてもある程度、感染制御に成功してきたのも事実である。しかし、新たな変異株が次々と報告され、東京オリンピック開催といった世界的イベントが控えている状況においては、ワクチンに頼るだけではなく、社会的検査、すなわち、誰でも何処でも何時でも受けられるPCR検査体制を拡充し、国民が安心して会食やイベントに参加できるような態勢を構築することが必要であろう。マスクなしで友人たちの笑顔を見ることが出来る日が一日でも早く来ることを願ってやまない。
[引用文献]
- Herrera LA, et al. Saliva is a reliable and accessible source for the detection of SARS-CoV-2. Int J Infect Dis. 2021 Apr;105:83-90. PMID: 33581365, DOI: 10.1016/j.ijid.2021.02.009.
- Barat B, et al. Pooled Saliva Specimens for SARS-CoV-2 Testing. J Clin Microbiol. 2021 Feb 18;59(3):e02486-20. PMID: 33262219, DOI: 10.1128/JCM.02486-20.
- Wyllie AL, et al. Saliva or nasopharyngeal swab specimens for detection of SARSCoV-2. N Engl J Med 2020; 383: 1283–1286. PMID:32857487, DOI:10.1056/NEJMc2016359.
- Medeiros da Silva RC, et al. Saliva as a possible tool for the SARS-CoV-2 detection: A review. Travel Med Infect Dis. Nov-Dec 2020;38:101920. PMID: 33220456, DOI: 10.1016/j.tmaid.2020.101920.
- Bastos ML, et al. The Sensitivity and Costs of Testing for SARS-CoV-2 Infection With Saliva Versus Nasopharyngeal Swabs: A Systematic Review and Meta-analysis. Ann Intern Med. 2021 Apr;174(4):501-510. PMID: 33428446, DOI: 10.7326/M20-6569.
- Butler-Laporte G, et al. Comparison of Saliva and Nasopharyngeal Swab Nucleic Acid Amplification Testing for Detection of SARS-CoV-2: A Systematic Review and Meta-analysis. JAMA Intern Med. 2021 Mar 1;181(3):353-360. PMID: 33449069, DOI: 10.1001/jamainternmed.2020.8876.
- La Scola B, et al. Viral RNA load as determined by cell culture as a management tool for discharge of SARS-CoV-2 patients from infectious disease wards. Eur J Clin Microbiol Infect Dis 2020; 39: 1059–1061. PMID:32342252, DOI:10.1007/s10096-020-03913-9.
- Bullard J, et al. Predicting infectious SARSCoV-2 from diagnostic samples. Clin Infect Dis 2020 Dec 17;71(10):2663-2666.PMID:32442256, DOI: 10.1093/cid/ciaa638.
- Singanayagam A, et al. Duration of infectiousness and correlation with RT-PCR cycle threshold values in cases of COVID-19, England, January to May 2020. Euro Surveill 2020; 25: 2001483. PMID:32794447, DOI:10.2807/1560-7917.ES.2020.25.32.2001483.
- Gniazdowski V, et al. Repeat COVID-19 molecular testing: correlation of SARS-CoV-2 culture with molecular assays and cycle thresholds. Clin Infect Dis. 2020 Oct 27. PMID: 33104776, DOI: 10.1093/cid/ciaa1616.
- Yamayoshi S, et al. Comparison of rapid antigen tests for COVID-19. Viruses 2020; 12: 1420. PMID:33322035, DOI:10.3390/v12121420.
- Oba J, et al. RT-PCR Screening Tests for SARS-CoV-2 with Saliva Samples in Asymptomatic People: Strategy to Maintain Social and Economic Activities while Reducing the Risk of Spreading the Virus. Keio J Med. 2021 Mar 19. PMID: 33746151, DOI: 10.2302/kjm.2021-0003-OA.
- Deka S, Kalita D. Effectiveness of Sample Pooling Strategies for SARS-CoV-2 Mass Screening by RT-PCR: A Scoping Review. J Lab Physicians. 2020 Dec;12(3):212-218. PMID: 33268939, DOI: 10.1055/s-0040-1721159.
- Watkins AE, et al. Increased SARS-CoV-2 Testing Capacity with Pooled Saliva Samples. Emerg Infect Dis. 2021 Apr;27(4):1184-1187. PMID: 33755009, DOI: 10.3201/eid2704.204200.
- Regen F, et al. A simple approach to optimum pool size for pooled SARS-CoV-2 testing. Int J Infect Dis. 2020 Nov;100:324-326. PMID: 32866638, DOI: 10.1016/j.ijid.2020.08.063.
- Bish DR, et al. A robust pooled testing approach to expand COVID-19 screening capacity. PLoS One. 2021 Feb 8;16(2):e0246285. PMID: 33556129, DOI: 10.1371/journal.pone.0246285.
- van Kampen JJA, et al. Duration and key determinants of infectious virus shedding in hospitalized patients with coronavirus disease-2019 (COVID-19). Nat Commun. 2021 Jan 11;12(1):267. PMID: 33431879, DOI: 10.1038/s41467-020-20568-4.
- Hogan CA, et al. High Frequency of SARS-CoV-2 RNAemia and Association With Severe Disease. Clin Infect Dis. 2021 May 4;72(9):e291-e295. PMID: 32965474, DOI: 10.1093/cid/ciaa1054.
- Mizumoto K, et al. Estimating the asymptomatic proportion of coronavirus disease 2019 (COVID-19) cases on board the Diamond Princess cruise ship, Yokohama, Japan, 2020. Euro Surveill. 2020 Mar;25(10):2000180. PMID: 32183930, DOI: 10.2807/1560-7917.ES.2020.25.10.2000180.
- Yang Q, et al. Just 2% of SARS-CoV-2-positive individuals carry 90% of the virus circulating in communities. Proc Natl Acad Sci U S A. 2021 May 25;118(21):e2104547118. PMID: 33972412, DOI: 10.1073/pnas.2104547118.
- Mina MJ, et al. Rethinking Covid-19 Test Sensitivity – A Strategy for Containment. N Engl J Med. 2020 Nov 26;383(22):e120. PMID: 32997903, DOI: 10.1056/NEJMp2025631.
- Larremore DB, et al. Test sensitivity is secondary to frequency and turnaround time for COVID-19 screening. Sci Adv. 2021 Jan 1;7(1):eabd5393. PMID: 33219112, DOI: 10.1126/sciadv.abd5393.
- Davies NG, et al. Estimated transmissibility and impact of SARS-CoV-2 lineage B.1.1.7 in England. Science. 2021 Apr 9;372(6538):eabg3055. PMID: 33658326, DOI: 10.1126/science.abg3055.
- Kim YJ, et al. The Impact on Infectivity and Neutralization Efficiency of SARS-CoV-2 Lineage B.1.351 Pseudovirus. Viruses. 2021 Apr 7;13(4):633. PMID: 33917138, DOI: 10.3390/v13040633.
- Faria NR, et al. Genomics and epidemiology of the P.1 SARS-CoV-2 lineage in Manaus, Brazil. Science. 2021 May 21;372(6544):815-821. PMID: 33853970, DOI: 10.1126/science.abh2644.
- Volz E, et al. Assessing transmissibility of SARS-CoV-2 lineage B.1.1.7 in England. Nature. 2021 May;593(7858):266-269. PMID: 33767447, DOI: 10.1038/s41586-021-03470-x. Epub 2021 Mar 25.
- Mahase E. Covid-19: What have we learnt about the new variant in the UK? BMJ. 2020 Dec 23;371:m4944. PMID: 33361120, DOI: 10.1136/bmj.m4944.
- 国立感染症研究所「感染・伝播性の増加や抗原性の変化が懸念される 新型コロナウイルス(SARS-CoV-2)の新規変異株について (第8報)
- Hoffmann M, et al. SARS-CoV-2 variants B.1.351 and P.1 escape from neutralizing antibodies. Cell. 2021 Apr 29;184(9):2384-2393.e12. PMID: 33794143, DOI: 10.1016/j.cell.2021.03.036.
- Vaidyanathan G. Coronavirus variants are spreading in India – what scientists know so far. Nature. 2021 May;593(7859):321-322. PMID: 33976409, DOI: 10.1038/d41586-021-01274-7.
- Cherian S, et al. Convergent evolution of SARS-CoV-2 spike mutations, L452R, E484Q and P681R, in the second wave of COVID-19 in Maharashtra, India. bioRxiv 2021.04.22.440932; DOI: https://doi.org/10.1101/2021.04.22.440932
- Hoffmann M, et al. SARS-CoV-2 variant B.1.617 is resistant to Bamlanivimab and evades antibodies induced by infection and vaccination. bioRxiv 2021.05.04.442663; DOI: https://doi.org/10.1101/2021.05.04.442663
- Bernal JL, et al. Effectiveness of COVID-19 vaccines against the B.1.617.2 variant. medRxiv 2021.05.22.21257658; DOI: https://doi.org/10.1101/2021.05.22.21257658